孤立電子対
原子の最外殻の電子対のうち、共有結合に関与していない電子対
(非共有電子対から転送)
この記事は英語版の対応するページを翻訳することにより充実させることができます。(2024年6月) 翻訳前に重要な指示を読むには右にある[表示]をクリックしてください。
●英語版記事を日本語へ機械翻訳したバージョン︵Google翻訳︶。
●万が一翻訳の手がかりとして機械翻訳を用いた場合、翻訳者は必ず翻訳元原文を参照して機械翻訳の誤りを訂正し、正確な翻訳にしなければなりません。これが成されていない場合、記事は削除の方針G-3に基づき、削除される可能性があります。
●信頼性が低いまたは低品質な文章を翻訳しないでください。もし可能ならば、文章を他言語版記事に示された文献で正しいかどうかを確認してください。
●履歴継承を行うため、要約欄に翻訳元となった記事のページ名・版について記述する必要があります。記述方法については、Wikipedia:翻訳のガイドライン#要約欄への記入を参照ください。
●翻訳後、 {{翻訳告知|en|Lone pair|…}}をノートに追加することもできます。
●Wikipedia:翻訳のガイドラインに、より詳細な翻訳の手順・指針についての説明があります。
|
孤立電子対︵こりつでんしつい、英: lone pair︶とは、原子の最外殻の電子対のうち、共有結合に関与していない電子対のこと。それゆえ、非共有電子対︵ひきょうゆうでんしつい、英: unshared electron pair︶とも呼ばれる。

水酸化物イオンの孤立電子対
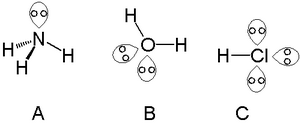
左から、アンモニア、水、塩化水素の孤立電子対
英語では、lone pairなので、﹁lp﹂と略すこともある。
量子力学的には、電子軌道はエネルギー準位の低いものから占有され、且つ一つの軌道にはスピンの異なる電子しか入ることができない。電子のスピンは+1/2と-1/2の二種類のみであるので対を成して軌道を占有することになる。分子軌道上にない電子はその原子のみに属するので、これを孤立電子対と呼ぶ。有機電子論では反応機構の要素として孤立電子対に独特の役割を想定していたが、量子論を中心とした現代の反応論では﹁共有結合に関与していない電子対﹂以上の意味はない。
孤立電子対の電子は金属やルイス酸性物質に配位することが可能であり、孤立電子対を持つ化合物は配位子やルイス塩基として働くことができる。


関連項目
編集