骨髄異形成症候群
表示
| 骨髄異形成症候群のデータ | |
| ICD-10 | D461〜464、D469 |
| 統計 | |
| 世界の患者数 | |
| 日本の患者数 | 9,000人 (2008年) |
| 関連学会 | |
| 日本 | 日本血液学会 |
| 世界 | アメリカ血液学会 |
| この記事はウィキプロジェクトの雛形を用いています | |
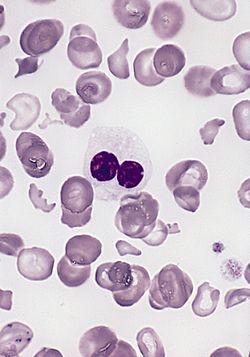
骨髄異形成症候群︵こつずいいけいせいしょうこうぐん、英: myelodysplastic syndromes、略称: MDS︶とは骨髄機能の異常によって前白血病状態となり、造血障害を起こす症候群である。

5q-症候群による異常な巨核球
病態[編集]
骨髄に造血幹細胞の前腫瘍細胞である異型クローンが生じ、正常幹細胞を凌駕して増殖する結果として正常の造血が抑制される。また異型クローンから造られる血球細胞は異常細胞なので末梢血に出る前に分解されるが、この様な無駄な造血を無効造血と言う。形成される血球は形態も異常で寿命も短い。白血病との関係[編集]
MDSの異常クローンはアポトーシスが亢進している。異常クローンが骨髄を占拠する結果として骨髄は過形成になるが、アポトーシスが亢進しているので血球減少をおこす。この状態で異常クローンの遺伝子にさらに傷がつくとアポトーシス耐性を獲得するクローンができる。この場合急性骨髄性白血病になる。このメカニズムがあるが故に、MDSを前白血病状態と呼ぶ者もいる。分類[編集]

FAB分類[編集]
2000年より前にはFAB分類が用いられていた。 ●不応性貧血 (RA) ●環状鉄芽球を伴う不応性貧血 (RARS) ●芽球増加を伴う不応性貧血 (RAEB) ●移行期の芽球増加を伴う不応性貧血 (RAEB-t) ●慢性骨髄単球性白血病 (CMML) その後、1999年から2001年にかけてWHOにて提唱され、WHO分類第3版として出版された分類では、慢性骨髄単球性白血病 (CMML) は骨髄異形成/骨髄増殖性疾患 (MDS/MPD) 群に分類された。WHO分類[編集]
2000年にWHOによって確立された新WHO分類が最も一般的である。同時に作成されたMDS 2000は新WHO分類に含まれるので、新WHO分類でのみ考慮すれば充分となる。2008年、WHOは遺伝学的な発見により基づいた新たな分類を発表した。2016年にWHO分類が改訂された[1]。2016年版[編集]
| サブタイプ | 異形成系統数 | 血球減少系統数 | 骨髄中の赤血球の環状鉄芽球の割合(%) | 末梢血または骨髄中の芽球の割合(%) AR: アウエル小体 |
従来型細胞遺伝学 | |||
|---|---|---|---|---|---|---|---|---|
| wtSF3B1 | mSF3B1 | BM | PB | AR | ||||
| MDS-SLD | 1 | 1または2 | 15 | 5 | 5 | 1 | - | |
| MDS-MLD | 2または3 | 1–3 | 15 | 5 | 5 | 1 | - | |
| MDS-RS-SLD | 1 | 1または2 | ≥15 | ≥5 | 5 | 1 | - | |
| MDS-RS-MLD | 2または3 | 1–3 | ≥15 | ≥5 | 5 | 1 | - | |
| MDS del(5q) | 1–3 | 1または2 | n.a. | n.a. | 5 | 1 | - | del(7)または-7を伴わない、1つの追加的な細胞遺伝学的異常を伴うまたは伴わない孤立したdel(5q) |
| MDS-EB-1 | 0–3 | 1–3 | n.a. | n.a. | 5–9 | 2–4 | - | |
| MDS-EB-2 | 0–3 | 1–3 | n.a. | n.a. | 10–19 | 5–19 | + | |
| MDS-U | 15 | 5 | 5 | 1 | - | |||
| (a) 末梢血中に1%の芽球 | 1–3 | 1–3 | n.a. | n.a. | 5 | 1 | - | |
| (b) 汎血球減少を伴うSLD | 1 | 3 | n.a. | n.a. | 5 | 1 | - | |
| (c) 決定的な細胞遺伝学的異常 | 0 | 1–3 | 15 | n.a. | 5 | 1 | - | 細胞遺伝学的異常を定義するMDS |
| RCC | 1–3 | 1–3 | 15 | ≤5 | 5 | 1 | - | |
2008年版[編集]
| 分類 | 末梢血中の 芽球の割合 |
骨髄中の 芽球の割合 |
特徴 | FAB分類 | |
|---|---|---|---|---|---|
| 単一血球系統の異形成を伴う不応性血球減少症(RCUD) | 不応性貧血(RA) | <1% | <5% | 骨髄で1血球系統で10%以上の細胞に異形成、 赤芽球のうち環状鉄芽球15%未満。 |
不応性貧血(RA) |
| 不応性好中球減少症(RN) | |||||
| 不応性血小板減少症(RT) | |||||
| 鉄芽球性不応性貧血 (RARS) | RARS | 赤芽球系の異形成のみ。環状鉄芽球が全赤芽球の15%以上を占めるもの。芽球5%未満。環状鉄芽球とはミトコンドリアに鉄が沈着し、プロシャ青染色で鉄顆粒が核に沿って核周の1/3以上に環状に配列したものである。 | RARS | ||
| RARS-T(暫定) | 血小板増加を伴うRARS。本質的には骨髄異形成-骨髄増殖性疾患であり、大抵はJAK2変異を持つ。 | ||||
| 多血球系異形成を伴う不応性血球減少症(RCMD) | RCMD | 2血球系統以上で10%以上の細胞に異形成。アウエル小体なし。環状鉄芽球が全赤芽球の15%未満。 | |||
| RCMD-RS | 環状鉄芽球を有するRCMD | ||||
| 芽球増加を伴う不応性貧血-1 (RAEB-I) | <5% | 5-9% | アウエル小体なし。 | RAEB | |
| 芽球増加を伴う不応性貧血-2 (RAEB-II) | 5-19% | 10-19% | 末梢血中のアウエル小体が5%未満。急性骨髄性白血病と区別するのが困難。 | ||
| 分類不能MDS (MDS-U) | <1% | <5% | 上記のいずれにも属さないもの。顆粒球系にのみ異形成が見られるものなど。 | ||
| 5q-症候群 | 染色体異常として5q-(5番染色体の長椀欠失)を有するタイプ。不応性貧血に類似するが、巨核球が小型で単核であるという特徴がある。最も白血病になりにくい。 | ||||
分類不能型骨髄異形成症候群[編集]
ほとんどの症例に対してWHOが提唱しているMDSの診断および分類のための基準が適用される。しかしながら、偶発症例は1つ以上のまれな特徴のために定義されたカテゴリーに分類することが困難である。
●アウエル小体が見られる芽球が5%未満のまれな症例。これらの症例は大抵RAMD︵多血球系異形成を伴う不応性貧血︶の特徴を有する。
●貧血を示さず孤立性好中球減少症あるいは孤立性血小板減少症を示し、単一の血球系に限定された異形成変化を示すMDSの偶発症例。不応性好中球減少症および不応性血小板減少症という用語がこれらの症例を説明するために使われることがある。貧血を伴わない好中球減少症あるいは血小板減少症の患者におけるMDSの診断は慎重に行われなければならない。
●通常の血球減少の代わりに白血球増加あるいは 血小板増加を時折示すことがあるRAあるいはRAEBの患者。
病態生理[編集]
MDSは放射線やベンゼンといった環境暴露によって引き起こされる可能性がある。その他の危険因子も一貫性なく報告されている。しかしながら、特定の原因の決定的証拠を確定することはできない。二次MDSはがん治療、通常は放射線治療とブスルファン、ニトロソウレア、プロカルバジンといった放射線模倣アルキル化剤の組み合わせ︵潜伏期5-7年︶、またはDNAトポイソメラーゼ阻害剤との組合わせ︵潜伏期2年︶の遅発性毒性として起こる。免疫抑制治療後の後天性再生不良性貧血およびファンコーニ貧血はどちらもMDSへと進行し得る。 MDSは多能性骨髄幹細胞における突然変異に起因すると考えられているが、これらの病気の原因となる特異的異常については依然として不明なところが多いままである。血液の前駆細胞の分化が損われており、骨髄細胞におけるアポトーシス性細胞死が顕著に増加している。異常細胞のクローン性増殖によって分化能を失った細胞の生産が起こる 。骨髄芽球の総割合が特定の値︵WHOでは20%︶を超えたとすると、急性骨髄性白血病︵AML︶への移行が起こったと診断される。MDSからAMLへの進行は、最初に正常細胞において一連の突然変異が起こり、がん細胞へと転換するというクヌードソン仮説の実例である。白血病への移行の認識は歴史的に重要であったが、MDSに帰せられる病的状態と死亡の相当な割合はAMLへの移行からではなく、むしろ全てのMDS患者において見られる血球減少症に起因する。貧血がMDS患者において最も一般的な血球減少症であるが、輸血が容易に受けられるため、MDS患者が深刻な貧血から損傷を受けることはまれである。血球減少に起因するMDS患者における2つの最も深刻な合併症は︵血小板減少による︶出血と︵白血球減少による︶感染症である。長期的な濃厚赤血球の輸血は鉄過剰症を引き起こす。遺伝学[編集]
MDS治療のためにアメリカ食品医薬品局(FDA) によって認可された3種類の薬の内の2種類の成功によってMDSにおけるDNA構造のエピジェネティク変化が認識された。適切なDNAメチル化は増殖遺伝子の制御に決定的に重要な意味を持ち、DNAメチル化制御が失われることによって無制御な細胞増速と血球減少症が引き起こされ得る。近年承認されたDNAメチルトランスフェラーゼ阻害剤は、造血幹細胞核におてより秩序だったDNAメチル化様式を作ることによってこの機構をうまく利用し、それによって正常な血球数に戻し、MDSの急性白血病への進行を遅らせる。 一部の著者らは、長い期間をかけたミトコンドリアの機能の消失が造血幹細胞におけるDNA変異を蓄積させ、これが高齢の患者におけるMDSの発症率の上昇の主な原因であると提唱している。研究者らは、MDSにおけるミトコンドリアミトコンドリア機能不全の証拠として環状鉄芽球におけるミトコンドリアの鉄沈着の蓄積を指摘する[2]。5q-症候群[編集]
少なくとも1974年以降、5番染色体長腕の欠損が造血幹細胞の異形成異常と関連することが知られている[3][4]。2005年までに、抗がん剤のレナリドミドが5q-症候群のMDS患者に有効であることが認知され[5]、2005年12月に米国FDAはレナリドミドをこの症状に対して承認した。孤立性5q-、低IPSSリスク、輸血依存性の患者がレナリドミドに最もよく反応する。典型的に、これらの患者の予後は好ましく、生存期間の中央値は63か月である。レナリドミドは二重の作用を持つ。一つは5q-の患者において悪性クローン数を低下させることによる作用、もう一つは5q欠損を持たない患者で見られるように健康な赤血球系細胞のよい良い分化を誘導することによる作用である。スプライシング因子変異[編集]
スプライシング因子における変異がMDSの症例の40-80%、特に環状鉄芽球を有する患者において見られる[6]。IDH1およびIDH2変異[編集]
イソクエン酸デヒドロゲナーゼ1および2︵IDH1およびIDH2︶をコードする遺伝子における変異がMDS患者の10-20%で起こっており[7]、低リスクMDSにおける予後悪化因子である[8]。IDH1/2変異は病気の悪性度の上昇と共に上昇するため、IDH1/2変異がMDSのより悪性な病気状態への進行の重要なけん引役であることが示唆されている[8]。疫学[編集]
男女比は1.5〜1.7と男性に多い。発症は40代から次第に増加し、高齢者に多い疾患であるため、先進国では平均年齢の増加に伴い患者数が増加傾向にある。症状[編集]
発症時の症状は乏しい。無症状かあるいは赤血球の産生が低下して慢性の貧血を来たす。貧血の型は一定せず、大球性から小球性までとりえる。白血球減少が高度な例で感染症の合併、血小板減少が高度な例で出血傾向が見られるものの、血液検査で白血球減少、血小板減少、汎血球減少が偶然発見されることも多い。合併症[編集]
最も重要なものは白血病である。高リスク群に分類される型では、急性白血病︵特に急性骨髄性白血病︶へ移行する率が高い。 他に、白血球減少に伴う感染症も重要なものの一つである。- 鉄過剰症
- 骨髄異形成症候群の治療で、赤血球輸血を受け鉄が過剰に体に取り込まれることによって発症する。特有の自覚症状は無く、進行すると肝障害や心不全などの臓器障害を引き起こす危険性がある。輸血が40単位を超えた場合、発症するリスクが高くなる。
- 1年以上の予後が見込まれる場合は、鉄キレート療法も行われる。
検査[編集]
血液検査[編集]
- 末梢血塗沫染色標本検査
- 造血低下と無効造血により汎血球減少または2血球減少を示す。正球性ないし大球性貧血が見られる。RARSでは例外的に小球性低色素性赤血球が混在する。
- 骨髄塗沫メイ・ギムザ染色標本検査
- 原則として正形成もしくは無効造血などによって過形成が見られる。一部低形成が見られるものもある。塗抹標本や骨髄生検で異形成が見られないか観察する。
- 染色体検査
- 様々な染色体異常が認められる。
- MDS診断用フローサイトメトリー
- 診断が難しい場合に有用だが、一部の病院でしか行えない。
- PNH血球検査
![[icon]](//upload.wikimedia.org/wikipedia/commons/thumb/1/1c/Wiki_letter_w_cropped.svg/20px-Wiki_letter_w_cropped.svg.png) この節の加筆が望まれています。
この節の加筆が望まれています。
診断[編集]
汎血球減少が見られた場合、まず骨髄異形成症候群を念頭に置く。次に腫瘍や膠原病などを除外し、その上で骨髄塗抹標本で形態異常を確認し診断する。しかし形態異常の確認には検査者の主観が入りやすく、正確性に欠くことがある。これを補うために以下の補助検査が有用である。骨髄穿刺時に染色体検査をし、染色体異常が見られれば確度は高まる。また、一部の病院ではMDS診断用フローサイトメトリー検査が可能であり、骨髄異形成症候群に特徴的な異常が検出されれば診断の正確性があがる。
治療[編集]
軽症例では経過観察となり、基本的に対症療法が中心となる。好中球減少例には顆粒球コロニー刺激因子 (G-CSF) の投与を、赤血球減少例にはエリスロポエチン (EPO) の投与を行い、それぞれ極端な減少例には輸血療法で対処としていく。 重症例に対しては根治療法として、造血幹細胞移植を行う。異常クローンを根絶し、正常造血を回復させるのが目的である。 また、薬物治療としては以下が用いられる。 ●免疫抑制剤‥PNH︵発作性夜間血色素尿症︶血球陽性例・HLA-DR15症例に用いられる。 ●シクロスポリン ●ATG︵抗胸腺細胞グロブリン︶ ●アザシチジン︵ビダーザ︶‥DNAメチル化阻害薬。 ●レナリドミド︵商品名レブラミド︶‥サリドマイド誘導体で5番染色体長腕欠損 (del 5q)の 症例に用いられる。 ●サイトカイン療法‥ただし、日本国内未承認[9]。予後[編集]
予後不良である。予後良好の不応性貧血で生存年数は約5年、予後不良のタイプでは1年程度である。骨髄移植実施例での長期生存率は不応性貧血では40%から60%、RAEBでは20%から30%程度である。歴史[編集]
概念[編集]
このような病態を示す造血障害の存在は古くから知られていたが、骨髄異形成症候群として確立したのは1982年である。この確立に尽力したDr. John M. Bennettらは国際MDS財団を設立し、その後のMDS研究の進歩を推進した。現在、全世界で200施設あまりが、国内では5施設が、MDSに関する優れた研究・診療施設 (MDS Centers of Excellence) として国際MDS財団に認定されている。さらに国際MDS財団は、MDS患者に対する有用な情報の提供︵現在の治療法の解説、新薬の臨床試験の情報提供、最寄りのMDS Centers of Excellenceの情報提供など︶を行うとともに、Global Patient Support Groups︵グローバルMDS患者サポートグループ︶のスポンサーとして、MDS患者サポートグループの立ち上げと運営を支援している。日本でも日本MDS患者サポートグループが設立され、MDSの方々に情報提供などの支援を行っている。各国において[編集]
日本[編集]
高齢化に伴い、患者数は増加傾向にある。脚注[編集]
- ^ Hasserjian RP, et al. (2017). “Myelodysplastic syndromes”. In Swerdlow SH, et al. eds.. WHO Classification of Tumours of Haematopoietic and Lymphoid Tissues. Lyon: IARC. pp. pp.98-106
- ^ “Mitochondrial ferritin expression in erythroid cells from patients with sideroblastic anemia”. Blood 101 (5): 1996–2000. (2003). doi:10.1182/blood-2002-07-2006. PMID 12406866.
- ^ Bunn HF (1986). “5q- and disordered haematopoiesis”. Clinics in haematology 15 (4): 1023–35. PMID 3552346.
- ^ “Distinct haematological disorder with deletion of long arm of no. 5 chromosome”. Nature 251 (5474): 437–8. (1974). doi:10.1038/251437a0. PMID 4421285.
- ^ “Efficacy of lenalidomide in myelodysplastic syndromes”. N. Engl. J. Med. 352 (6): 549–57. (2005). doi:10.1056/NEJMoa041668. PMID 15703420.
- ^ Rozovski U, Keating M, Estrov Z (2012) The significance of spliceosome mutations in chronic lymphocytic leukemia. Leuk Lymphoma
- ^ Molenaar, Remco J.; Radivoyevitch, Tomas; Maciejewski, Jaroslaw P.; van Noorden, Cornelis J. F.; Bleeker, Fonnet E. (2014-12-01). “The driver and passenger effects of isocitrate dehydrogenase 1 and 2 mutations in oncogenesis and survival prolongation”. Biochimica et Biophysica Acta (BBA) - Reviews on Cancer 1846 (2): 326–341. doi:10.1016/j.bbcan.2014.05.004.
- ^ a b Molenaar, R J; Thota, S; Nagata, Y; Patel, B; Clemente, M; Przychodzen, B; Hirsh, C; Viny, A D et al.. “Clinical and biological implications of ancestral and non-ancestral IDH1 and IDH2 mutations in myeloid neoplasms”. Leukemia 29 (11): 2134–2142. doi:10.1038/leu.2015.91.
- ^ 造血器腫瘍診療ガイドライン 日本血液学会
外部リンク[編集]
- 骨髄異形成症候群(国立がんセンター がん情報サービス 一般の方向けサイト 2006年10月10日) - ウェイバックマシン(2016年6月13日アーカイブ分)
- 不応性貧血(骨髄異形成症候群)特定疾患情報(難病情報センター、2008年5月1日) - ウェイバックマシン(2009年8月26日アーカイブ分)
- 国際MDS財団
- 日本MDS患者サポートグループ (Japan MDS Patient Support Group)
