エスゾピクロン
(ルネスタから転送)
 | |
 | |
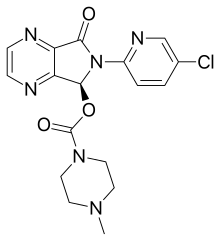
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| 胎児危険度分類 |
|
| 法的規制 |
|
| 投与経路 | 1,2,3 mg錠 経口投与 |
| 薬物動態データ | |
| 代謝 | 肝臓 |
| 半減期 | 6時間以下 |
| 排泄 | 尿 |
| 識別 | |
| CAS番号 | 138729-47-2 |
| ATCコード | N05CF04 (WHO) |
| PubChem | CID: 969472 |
| DrugBank |
APRD00431 |
| 化学的データ | |
| 化学式 | C17H17ClN6O3 |
| 分子量 | 388.808 g/mol |
エスゾピクロン︵英語: Eszopiclone︶は、シクロピロロン系の睡眠障害改善剤であり、非ベンゾジアゼピン系の超短時間作用型睡眠薬として知られている。日本では2012年よりルネスタが販売されている。ラセミ体であるゾピクロンを光学分割して得られたS体で、GABAA受容体に作用することで催眠作用などを有する。
ヨーロッパでは、ゾピクロンに似すぎていると判断され、販売されていない。2014年には、アメリカ食品医薬品局(FDA)は、翌日への持ち越し効果による自動車の運転に対する機能障害から、推奨開始使用量を1mgとした。ゾピクロンよりも使用量が少ないため軽減されているが、代謝産物が苦味をもつため、排出されるまで長時間苦味が持続する。
連用により依存症、急激な量の減少により離脱症状を生じることがある[1]。薬機法における習慣性医薬品である[2]。ゾピクロンとは異なり、麻薬及び向精神薬取締法における向精神薬に指定されない。
歴史[編集]
大日本住友製薬のアメリカ合衆国法人の子会社である、サノビオン・ファーマシューティカルズ︵旧‥セプラコール︶が創薬した。ラセミ体であるゾピクロンの (S)-鏡像異性体であり、ゾピクロン同様、GABAA受容体に作用し効果を示す。日本では2007年︵平成19年︶からエーザイがライセンス契約を結び、開発ならびに販売に関する権利を取得した[3]。 2011年︵平成23年︶には、厚生労働省薬事・食品衛生審議会より承認されている。2012年︵平成24年︶4月18日、エーザイよりルネスタ錠として、1mg・2mg・3mgが発売された。2021年2月15日に後発医薬品が承認され、6月に薬価追補収載、発売される[4]。 ルネスタの後発医薬品であるエスゾピクロン﹁DSEP︵販売元:第一三共エスファ︶﹂各mgのパッケージにはと就寝前服用や不眠症治療薬の説明と共に眠る顔のイラストが書かれている。薬理作用[編集]
GABAA受容体複合体に対する結合親和性︵Ki値︶は、エスゾピクロンが22 nmoL/L、ゾピクロンが42 nmol/L、また、Cl-チャネルに対する結合親和性は、エスゾピクロンが10 nmol/L、ゾピクロンが25 nmol/Lで、いずれもゾピクロン結合親和性の本体はエスゾピクロンである[5]。エスゾピクロンは、マウス、ラット及びサルにおいて、抗不安作用及び鎮静作用を示した[6]合成[編集]
ラセミ混合物︵R体とS体︶であるゾピクロンを光学分割して得られたS体が、エスゾピクロンである。効能・効果[編集]
●不眠症副作用[編集]
日本では2017年3月に﹁重大な副作用﹂の項に、連用により依存症を生じることがあるので用量と使用期間に注意し慎重に投与し、急激な量の減少によって離脱症状が生じるため徐々に減量する旨が追加され、厚生労働省よりこのことの周知徹底のため関係機関に通達がなされた[1]。 アメリカ食品医薬品局(FDA)は2014年5月15日付けの通知で、エスゾピクロンの推奨開始用量を1mgに変更した。翌日への持ち越し効果として、自動車の運転や記憶に関わる機能障害が生じる可能性が確認されたためとしている[7][8]。 代謝産物が苦味を持つため、口の中を通り抜けた後も苦みを感じるが、ゾピクロンよりも使用量が少ないため、その苦味は弱くなる。副作用の﹁苦み﹂は、添付文書およびインタビューフォームには﹁味覚異常︵不快な味︶﹂と記載されている。出典[編集]
(一)^ ab厚生労働省医薬・生活衛生局安全対策課長﹃催眠鎮静薬、抗不安薬および抗てんかん薬の﹁使用上の注意﹂改訂の周知について ︵薬生安発0321第2号︶﹄︵pdf︶︵プレスリリース︶。2017年3月25日閲覧。、および、“使用上の注意改訂情報︵平成29年3月21日指示分︶”. 医薬品医療機器総合機構 (2017年3月21日). 2017年3月25日閲覧。
(二)^ 厚生省﹃薬事法第50条第9号の規定に基づき習慣性があるものとして厚生労働大臣の指定する医薬品 通知本文﹄︵プレスリリース︶厚生労働省。2014年2月16日閲覧。
(三)^ ﹃睡眠導入剤﹁エスゾピクロン﹂の日本におけるライセンス契約を米国セプラコール社と締結﹄︵プレスリリース︶エーザイ、2007年7月27日。2011年12月12日閲覧。
(四)^ “厚労省・後発品承認 初後発は12成分 サインバルタ後発品に17社40品目”. ミクスonline (2021年2月16日). 2021年4月16日閲覧。
(五)^ ルネスタ錠 インタビューフォーム
(六)^ “医療用医薬品 : ルネスタ”. 2024年3月6日閲覧。
(七)^ 不眠症治療薬﹁エスゾピクロン﹂の用量を1mgに変更-FDA︵QLifePro、2014年05月30日︶
(八)^ FDA Drug Safety Communication: FDA warns of next-day impairment with sleep aid Lunesta (eszopiclone) and lowers recommended dose (FDA, 2014-5-15)
