大腸癌
表示
(結腸がんから転送)
| 大腸癌 | |
|---|---|
 | |
|
胃 (Stomach) と直腸 (Rectum) と 結腸 (Colon) の図 | |
| 概要 | |
| 診療科 | 腫瘍学 |
| 分類および外部参照情報 | |
| ICD-10 | C18-C20 |
| ICD-9-CM | 153.0-154.1 |
| ICD-O | M8140/3 (95%の事例) |
| OMIM | 114500 |
| DiseasesDB | 2975 |
| MedlinePlus | 000262 |
| eMedicine | med/413 med/1994 ped/3037 |
| Patient UK | 大腸癌 |
| KEGG 疾患 | H00020 |
大腸癌︵だいちょうがん、英語: Colorectal cancer[注釈 1]、ドイツ語: Kolorektales Karzinom︶は、大腸︵盲腸、結腸、直腸︶に発生する癌腫である[1]。肛門管に発生するものを含めることもある。
正式には部位別に盲腸癌︵もうちょうがん、Cecum cancer︶、結腸癌︵けっちょうがん、Colon cancer︶、直腸癌︵ちょくちょうがん、Rectum cancer︶と称される。
徴候や症状には、血便、腸の動きの変化、体重の減少、常時の疲労感などがある[2]。
男女で症状に性差があり、男性は、比較的肛門に近い位置に出っ張った腫瘍が、女性は肛門から離れた大腸の奥に扁平な腫瘍ができる。このため女性は検査で発見しづらく悪性度が高く女性死亡要因1位につながっていることが指摘されている[3]。
概要[編集]
ほとんどの結腸直腸癌は老年および生活習慣の要因によるもので、遺伝的疾患による症例はごくわずかである[4][5][6]。他のリスク因子には、食事、肥満、喫煙、運動不足などがある[4]。リスクを増大させる食事は赤身肉、加工肉、アルコールなどである[4][7][8]。他のリスク因子には炎症性腸疾患があり、クローン病および潰瘍性大腸炎を含む[4]。遺伝性疾患として原因となりえるものは家族性大腸腺腫症、遺伝性非ポリポーシス大腸癌であるが、これらは5%未満である[4][5]。典型的には当初はしばしば良性腫瘍であり、ポリープの形をとりえ、時を経てがんとなる[4]。 診断は大腸内視鏡検査によって行われ、サンプルを採取することで判別される[2]。転移進行を確認するために医用イメージングが行われる[1]。検査の一つであるスクリーニングは結腸直腸癌による死を予防および軽減するのに有効である[9]。スクリーニングは50歳から75歳から始めることが勧められる[9]。 世界的には、大腸癌はがんの中で3番目に多く、全症例の10%を占めている[10]。2012年には140万人の新たな症例が発生し、694,000人が死亡した[10]。先進国では一般的であり、全症例の65%以上を占める[4]。女性より男性のほうが多く発症する[4]。疫学[編集]

データなし
2.5人以下
2.5人から5人
5人から7.5人
7.5人から10人
10人から12.5人
12.5人から15人
15人から17.5人
17.5人から20人
20人から22.5人
22.5人から25人
25人から27.5人
27.5人以上
世界では毎年100万人以上の人々が大腸癌を発症する[12]。死者数は1990年には49万人、2010年には約715,000人であった[13]。
日本では女性のがんの死亡率の1位、男性では3位を占め、2015年には男性でも2位に上昇すると予想されている[14][15]。アメリカ合衆国においては、3番目に多い癌で、癌死の原因として2番目に多く、生涯に大腸癌に罹患する確率は約7%である。日本でも胃癌を追い越し肺癌についで2番目に多くなっている。
| 死亡数 (2017年) | 罹患数 (2014年) | |||||
|---|---|---|---|---|---|---|
| 男 | 女 | 男女 | 男 | 女 | 男女 | |
| 1位 | 肺 | 大腸 | 肺 | 胃 | 乳房 | 大腸 |
| 2位 | 胃 | 肺 | 大腸 | 肺 | 大腸 | 胃 |
| 3位 | 大腸 | 膵臓 | 胃 | 大腸 | 胃 | 肺 |
| 4位 | 肝臓 | 胃 | 膵臓 | 前立腺 | 肺 | 乳房 |
| 5位 | 膵臓 | 乳房 | 肝臓 | 肝臓 | 子宮 | 前立腺 |
症状[編集]
一般に早期大腸癌であれば自覚症状はなく、健康診断や人間ドックで発見される。症状が全く現れない場合も少なくない。進行大腸癌でも環周度[17]が1/4以下ならば症状はほとんどない。1/2周を超えると腸内容の通過障害を起こす場合がある。
左側結腸に存在すると便通異常、腹痛、腹部膨満感などがあり、血便を伴うこともある。しかし、右側結腸ではこれらの症状は乏しく貧血、体重減少、腫瘤触知などの症状となる。これは上行結腸では内容物がまだ液体であるからであると説明されている。左側結腸の全周性病変になると排便困難、便秘、イレウスを起こすこともある。
危険因子[編集]
以下のものが報告されている。
大腸癌に罹る家系
特に55歳以前の罹患や癌の多発の場合、顕著である。
年齢
大腸癌に進行するリスクは年齢とともに増加する。その多くは60歳代から70歳代で後期がんが発見されるが、早期発見のためには40歳以降は定期的な検診が必要であるとされる[18]。
癌の既往歴
卵巣癌、子宮癌、乳がんに罹患した婦人は、大腸癌に進行するリスクが増大する。
家族性大腸腺腫症︵家族性大腸ポリポーシス、Familial adenomatous polyposis;FAP︶
全大腸切除を施されない場合はほぼ100%が癌に進行する。
潰瘍性大腸炎︵Ulcerative colitis︶
長期罹患で寛解がコントロールされていない症例に多く、全大腸切除を施されない場合には25年後でおよそ30%が大腸癌となる。
腸内細菌である硫化水素産生菌が産生する硫化水素が潰瘍性大腸炎の原因ではないかとの指摘がある。大腸の粘膜に硫化水素を代謝する酵素が存在するが、その処理量以上の硫化水素に大腸がさらされることが潰瘍性大腸炎の原因となるのではないかとの指摘がされている[19]。硫化水素はミトコンドリアに所在するシトクロムcオキシダーゼを阻害することにより毒性を発現する。高濃度の硫化水素に曝露されることでアポトーシス関連蛋白質であるcaspase3の活性化、ミトコンドリアからのシトクロムcの遊離が見られ、ミトコンドリアを介したアポトーシスが誘導される可能性があると報告されている[20][21]。
遺伝性非ポリポーシス大腸癌︵Hereditary nonpolyposis colorectal cancer;HNPCC︶
大腸癌や他臓器癌の高リスク群であるため定期的なスクリーニングが推奨される。
過体重・肥満
リスクが高まることが確実視されている。
男性で肥満だと大腸癌になりやすい[22]。
赤肉、加工肉︵ベーコン、ハム、ソーセージ︶
赤肉の摂取と大腸がんのリスクの増加が指摘されている[23]。がん予防10か条︵世界がん研究基金︶では﹁肉︵牛・豚・羊︶を制限し、加工肉︵ハム、ベーコン、サラミ、燻製肉、熟成肉、塩蔵肉︶は避ける。獣肉より、鶏肉や魚が推奨される。ゴール:肉は週300g以下に。推奨‥赤肉は週500g以下に。﹂と指摘されている[24]。IARC発がん性リスク一覧の発がん性があるとされるグループ1に加工肉が、おそらく発がん性がある2Aに赤身肉が追加されている。
飲酒
確実なリスク。
1日平均1合以上の飲酒者は、お酒を飲まない人に比べて、大腸癌になりやすい[25][26]。
喫煙
喫煙は特に直腸癌のリスク上昇となる。
たばこを吸う人は、吸わない人に比べて、大腸癌になりやすい[25]。
食事バランス
食物繊維をとり、動物性の食肉を減らすと大腸癌のリスクが低減すると言われており、食物繊維の摂取量が少ない︵平均約6g︶人のリスクが高くなる事は再確認されたが、食物繊維を多く摂取している人の肉食でリスクが高まるかは不明である。臨床的にはバランスの取れた食事は大切であるとされている[27][28]。
食物繊維摂取量の非常に少ない人で大腸癌リスクが高くなる可能性があるという報告がある[29]。
米国国立がん研究所の公開資料によると、﹁︵脂肪に富んだ︶大量の肉と大量のカロリーを摂取する人々は、特に大腸がんにおいて、がんの危険が増大することが図より見て取れる。﹂と指摘している[30]。
女性では、欧米型の食生活と大腸癌との関連が示唆されるという報告がある[31]。
過剰な胆汁酸
大腸癌患者群では正常な対照群に比して糞便中の一次胆汁酸および二次胆汁酸が高値を示した。また、大腸癌群がリトコール酸、デオキシコール酸、ケノデオキシコール酸、コール酸、ウルソデオキシコール酸の糞便中の総胆汁酸量でも高値を示した[32]。
マグネシウム
マグネシウム摂取量が多いグループの男性の大腸がんリスクが低いとの報告がある[33]。
C-ペプチド
C-ペプチドは、インスリン生成の際、インスリンの前駆体であるプロインスリンから切り放された部分を指す。男性では、C-ペプチド値が高いと大腸癌リスクが高くなる。C-ペプチドは男性の結腸癌と関連がある[34]。
高感度CRP
炎症の程度を示す高感度CRP︵C反応性蛋白︶の値が高いと、大腸癌リスクが高くなる[35]。
予防の可能性[編集]
検診 人の血液にのみ反応する免疫便潜血検査[36]は、スクリーニングとしての精度︵感度︶は低いが安価で検査への負担の少ない検診の方法として、現在日本では概ね︵自治体や各企業により違いがあるが︶35歳から40歳以上の人に対して推奨されている。健康診断の﹁大腸がん検診﹂はほとんどの場合これをさす。 便潜血は単回検査では感度は低いが、複数年に渡り毎年施行した場合の﹁プログラム感度﹂は95%以上であり、早期大腸癌発見と大腸癌死減少に有用である[37]。 血液検査による腫瘍マーカー︵CA 19-9やCEA︶による検診・人間ドックの方法もあるが、病期が進行するまで異常値を示さない場合が多く[38]早期発見にはつながりにくい。そのため、年齢や生活習慣および病歴などからみたハイリスクグループには、大腸内視鏡による検診が推奨[39]されている。 大腸癌検診を受けている人では、大腸癌による死亡率が低い[40]。 検査 ハイリスクグループや何らかの症状のある人は検査を受けるべきである。ほとんどの大腸がんは、腺腫性ポリープから発生する。これらの病変は大腸内視鏡検査で検知可能で除去可能である。50歳から始めて5年か10年毎に一度のこの内視鏡検査と病変の除去で、がん死のリスクを80%以上減少させることができる[41]。 米国全国総合がんネットワークによる現在のガイドラインにおける限り、大腸がんの家族歴がなく、腺種や炎症性腸疾患の病歴がない平均的な対象者で、5年毎のS字結腸の内視鏡検査と毎年の便潜血反応検査、あるいは、バリウム注腸二重造影検査は、10年毎の内視鏡検査よりも望ましい検査方法であるとされている。 生活習慣及び栄養 様々な国々での大腸がんの発生を比較すると、座り作業で、高カロリー食品の食べ過ぎ、多量の赤肉または加工肉の摂取は大腸がんの発生のリスクを高めることを強く示唆している。反面、健全な体重、適度な運動、良い栄養は一般的にがんのリスクを下げる。生活習慣を変えることにより大腸がんのリスクを60-80%下げることができると言われている[42]。 身体活動量の多い人で大腸癌リスクが低くなるという報告がある[43]。 便通は、大腸癌リスクと関係ない。下痢便は、直腸癌リスクと関連があるかもしれないという報告がある[44]。 野菜・果物をたくさん食べても大腸癌リスクは変わらず[45]。 果物、野菜、シリアルその他の食物繊維の多量の摂取は、大腸がんと腺種のリスクを下げると考えられてきた。この理論を検証するため16年にわたる88,757人を対象とした調査では、食物繊維の多い食事は大腸がんのリスクを下げてはいなかった[46]。2005年の別の調査でもその結果を支持している[47]。 ハーバード大学公衆衛生学部は﹁食物繊維の摂取は、健康効果のある健全な食事としてもてはやされ、心臓病、糖尿病、憩室疾患、便秘を含む様々な疾患のリスクを減少させていた。多くの人が信じていたにもかかわらず、食物繊維には大腸がんのリスクの減少の効果はほとんど認められなかった。﹂と発表している[48]。 世界保健機関︵WHO︶と国際がん研究機関 (IARC) による、﹁生活習慣とがんの関連﹂についてのリスクを下げるもの、リスクを上げるものに関する報告がある[49]。| 関連の強さ | リスクを下げるもの(部位) | リスクを上げるもの(部位) |
|---|---|---|
| 確実 | 身体活動(結腸) | たばこ(口腔、咽頭、喉頭、食道、胃、肺、膵臓、肝臓、腎臓、尿路、膀胱、子宮頸部、骨髄性白血病) 他人のたばこの煙(肺) 過体重と肥満(食道<腺がん>、結腸、直腸、乳房<閉経後>、子宮体部、腎臓) 飲酒(口腔、咽頭、喉頭、食道、肝臓、乳房)、 アフラトキシン(肝臓)、 鹹魚|中国式塩蔵魚(zh:鹹魚)(鼻咽頭) |
| 可能性大 | 野菜・果物(口腔、食道、胃、結腸、直腸) 身体活動(乳房) |
貯蔵肉(結腸、直腸) 塩蔵品および食塩(胃) 熱い飲食物(口腔、咽頭、食道) |
| 可能性あり データ不十分 | 食物繊維、大豆、魚、ω-3脂肪酸、 カロテノイド、ビタミンB2、ビタミンB6、 葉酸、ビタミンB12、ビタミンC、ビタミンD、 ビタミンE、カルシウム、亜鉛、セレン、 非栄養性植物機能成分 (例:アリウム化合物、フラボノイド、イソフラボン、リグナン) |
動物性脂肪 複素環式アミン 多環芳香族炭化水素 ニトロソ化合物 |
ビタミンD
アメリカ国立癌研究所は、ビタミンDの摂取が大腸がん及びその他のがんの予防効果について限定されているか証拠が不十分なので、大腸がん及びその他のがんの予防のためにビタミンDサプリメントの摂取を勧奨はしないとしている[51]。
ビタミンDの摂取が少ないと直腸がんのリスクが高かったとの報告がある[52]。
カルシウム
2つの無作為化比較試験[53][54]の国際コクラン共同計画によるメタ分析[55]によると、カルシウムは大腸腺腫性ポリープをある程度抑制し得るかもしれないことが発見された。
カルシウムとビタミンDの両方を多く摂取するグループで大腸癌のリスクが低下したとの報告がある[56]。
ある無作為化比較試験は、1,000mgのカルシウム成分と400IUのビタミンD3は大腸癌に何も効果を示さなかった[57]。
ω-3脂肪酸
魚由来のω-3脂肪酸およびトータルのω-3不飽和脂肪酸摂取量が多いグループの結腸癌リスクは低い。ω-6脂肪酸およびω-3/ω-6比は大腸癌のリスクと関連がみられない[58]。魚を食べても大腸癌のリスクが低下しないとの研究がある[59]。
アスピリン
後述の#化学療法を参照のこと。
ビタミンB6
ビタミンB6を多く摂取するグループで大腸癌のリスクが低下したとの報告がある[60]。
コーヒー
コーヒーは女性の浸潤結腸がんを予防したとの報告がある[61]。
酪酸菌及び酪酸
酪酸を生成する代表的な酪酸菌であるクロストリジウム・ブチリカムは、偏性嫌気性芽胞形成グラム陽性桿菌である。クロストリジウム属のタイプ種でもある。芽胞の形で環境中に広く存在しているが、特に動物の消化管内常在菌として知られている。日本では宮入菌と呼ばれる株が酪酸菌の有用菌株として著名であり、芽胞を製剤化して整腸剤として用いられている[62][63]。クロストリジウム属の一部の菌は酪酸菌として知られ、漬物の酪酸臭の原因となる[64]。酪酸は、腸管増殖因子として作用し、抗炎症作用を有し、傷害腸管の修復にも関与している[65]。腸内細菌が産生した酪酸が、ヒストンのアセチル化を促進し、p21遺伝子を刺激し、細胞サイクルをG1期で留めるタンパク質であるp21が大腸がんをG1期に留め置き大腸がんを抑制することが指摘されている[66][67]。酪酸生成能が高いButyrivibrio fibrisolvensをマウスに投与したところ、酪酸生成量が増加し、発癌物質で誘発した大腸前癌病変の形成が抑制され、大腸がんを予防、抑制する可能性が指摘されている[68]。大腸癌患者の糞便を健常者のものと比較すると有機酸濃度が低く、特にn-酪酸の濃度がとりわけ低値であったことが報告されている[69]。
病態[編集]
多くの大腸癌の発生に関する機序については大きく以下の2つが論じられている。 ●Adenoma carcinoma sequence︵腺腫-癌 発生︶ 腺腫︵大腸ポリープ︶から癌が発生し発展していくと考えられている。 ●de novo cancer︵新発生︶ 腺腫︵大腸ポリープ︶を経ずに何らかの要因によって癌が発生していくと考えられている。病理[編集]
大腸癌で最も多く見られるものは腺癌で、全体の95%も占める。他についても様々に存在する。詳細は「大腸ポリープ」を参照
検査[編集]
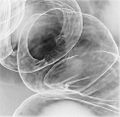
大腸癌は早期に発見できれば完全治癒の可能性が大きくなる。集団健診では費用対効果を考慮して通常は﹁便潜血反応﹂が行われる。反応が陽性であった場合、貧血などの異常がある場合、その他の大腸癌のハイリスクの場合は、癌をはじめとする大腸疾患の確定のため大腸内視鏡検査が行われる。 便潜血反応検査 (Fecal occult blood test;FOBT) ﹁化学的便潜血検査﹂と﹁免疫学的便潜血検査﹂がある。化学的便潜血検査は鉄分を含む食事によって検査結果が変化してしまうため、現在は免疫学的の﹁ヒトヘモグロビン法﹂が主流。多くの大腸癌検診の1次スクリーニングとして広く行われている。 ●大腸癌の既往歴や家族歴のある高リスク患者を対象に、免疫学的便潜血検査による診断精度を検討した論文を抽出しメタ解析した結果、大腸がんを検出するFITの感度は93%、特異度は91%と高かった[70]。 大腸内視鏡 (Colonoscopy) 内視鏡で直腸から回盲部まで挿入し病変を観察する。最近ではほぼ多くの場合に2次スクリーニングの確定診断目的に施行される。 バリウム注腸二重撮像法 (Double contrast barium enema;DCBE) 肛門からバリウム溶液を注入し、ついで空気を注入し、大腸や直腸の形状をX線で撮像する。直腸RSに発生した2型腫瘍の注腸バリウム像(高分化型管状腺癌)。
左と同じ症例の内視鏡像。
コンピュータ断層撮影法︵CT︶
X線診断法で進行癌の周囲への進展度合や他臓器転移の有無を検査するのに行われる。他の理由で実施されたCT断層撮影で進行大腸癌が発見されることもある。また内視鏡や透視とは異なり、腹部の断層撮影がなされていることから腸管の粘膜下病変を検出し、スキルスや粘膜下腫瘍、虫垂病変などの評価を行える。
現在、コンピューターの情報処理能力の進歩に伴いCT colonographyと呼ばれる仮想大腸内視鏡が普及しつつある。この方法は大腸をガスで膨らませ、肛門からカメラを入れ込むことなく、大腸部分を精密な3次元CT画像にする装置である。但し、事前の食事制限や下剤処理を受けることは同じ。唯一、陰性反応適中度が低いことが欠点とされる[71]が、これも科学的な根拠はないとされる。腸管に障害のある場合この検査法は、内視鏡検査の代替検査として有効である[72]。
血液検査
進行大腸癌があると貧血を来すことがよくある。貧血自体はありふれた疾患であるが、大腸癌がその原因の場合は進行癌のおそれがある。
腫瘍マーカー
癌胎児性抗原 (CEA) が代表的であるが、ほとんどが進行癌でしか異常値にならず、早期癌や大腸ポリープの発見指標にはならない。唾液から採取できるポリアミンを利用する検査手法も開発されている[73]。
バイオマーカー
病理組織検査や血液検査において、その後の治療選択の判断材料として、遺伝子検査が広く行われている。HER2、EGFR (HER1)、RAS、BRAF検査などが施行される。
病期[編集]
大腸癌の病期分類は主に局所浸潤の度合い、リンパ節浸潤の度合いあるいは遠隔転移の有無によって決定される。今日においては、日本では﹁大腸癌取り扱い規約﹂に基づく独自の病期分類を行っている。国際的にはTNM分類が病期分類に使用される。あるいは医者によっては以前から使用されていたデューク分類 (Duke's system) を使用する者もいる。
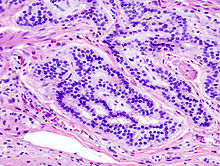
大腸腺癌の病理写真
漿膜を有する部位の壁深達度
m:癌が粘膜内にとどまり、粘膜下層に及んでいない。
sm:癌が粘膜下層にとどまり、固有筋層に及んでいない。
mp:癌が固有筋層にとどまり、これをこえていない。
ss:癌が固有筋層を超えているが漿膜表面に出ていない。
se:癌が漿膜表面に露出している。
si:癌が直接他臓器に浸潤している。
漿膜を有しない部位の壁深達度
m:癌が粘膜内にとどまり、粘膜下層に及んでいない。
sm:癌が粘膜下層にとどまり、固有筋層に及んでいない。
mp:癌が固有筋層にとどまり、これをこえていない。
A1:癌が固有筋層を超えているが、さらに深くは浸潤していない。
A2:癌が筋層を越えてさらに深く浸潤しているが他臓器に浸潤していない。
Ai:癌が直接他臓器に浸潤している。
リンパ節転移
n(-):リンパ節転移を認めない。
n1(-):第1群リンパ節に転移を認めない。
n1(+):第1群リンパ節に転移を認める。
n2(-):第2群リンパ節に転移を認めない。
n2(+):第2群リンパ節に転移を認める。
n3(-):第3群リンパ節に転移を認めない。
n3(+):第3群リンパ節に転移を認める。
n4(-):第4群リンパ節に転移を認めない。
n4(+):第4群リンパ節に転移を認める。
腹膜播種転移
P0:播種性転移を認めない。
P1:近接腹膜のみ播種性転移を認める︵合併切除可能なもの︶。
P2:遠隔腹膜に少数の転移を認めるもの。
P3:遠隔腹膜に多数の転移を認めるもの。
肝転移
H0:肝転移を認めない。
H1:一葉のみに肝転移を認める。
H2:両葉に少数散在性︵4個以内︶に転移を認める。
H3:両葉にわたり多数散在性︵5個以上︶に転移を認める。
肝以外の遠隔他臓器転移
M(-)‥遠隔他臓器転移が認められないもの。
M(+):遠隔他臓器転移が認められるもの。
ステージ分類[編集]
●ステージ0‥がんが粘膜の中にとどまっている[74]。 ●ステージⅠ‥がんが大腸の壁︵固有筋層︶にとどまっている[74]。 ●ステージⅡ‥がんが大腸の壁︵固有筋層︶外まで浸潤している[74]。 ●ステージⅢ‥リンパ節転移がある[74]。 ●ステージⅣ‥遠隔転移︵肝転移、肺転移︶または腹膜播種がある[74]。TNM分類[編集]
UICCのTNM分類の定義を次に示す。 ●T - 腸壁への浸潤度合い[74] ●T0 - がんの兆候は見出されない ●Tis- がんは粘膜内︵M︶にある︵腫瘍は存在しているが、浸潤はない︶ ●T1 - がんは存在しているが、粘膜下層︵SM︶にとどまる。 ●T2 - がんは筋固有層︵MP︶にとどまる。 ●T3 - がんは筋固有層を越えて漿膜下層または外膜までにとどまる。 ●T4a - がんは漿膜︵SE︶を越えた深さに達する︵漿膜表面に露出している︶。 ●T4b - がんが大腸周辺の他臓器にまで達する︵他臓器転移︶。 ●N - リンパ節浸潤の度合い ●N0 - リンパ節に浸潤は見られない ●N1 - 腸管傍リンパ節と中間リンパ節の転移総数が3個以下[75]。 ●N2 - 腸管傍リンパ節と中間リンパ節の転移総数が4個以上[75]。 ●N3 - 主リンパ節に転移を認める。下部直腸がんでは側方リンパ節に転移を認める[75]。 ●M - 転移の度合い ●M0 - 転移はない ●M1 - 転移が見られる 例えば患者が癌に罹患していなければT0N0M0となる。AJCC病期分類[編集]
●Stage 0 ●Tis, N0, M0 ●Stage I ●T1, N0, M0 ●T2, N0, M0 ●Stage IIA ●T3, N0, M0 ●Stage IIB ●T4, N0, M0 ●Stage IIIA ●T1, N1, M0 ●T2, N1, M0 ●Stage IIIB ●T3, N1, M0 ●T4, N1, M0 ●Stage IIIC ●いずれかのT, N2, M0 ●Stage IV ●いずれかのT, いずれかのN, M1大腸癌取り扱い規約による分類[編集]
まずは肉眼的分類として以下がある。 0型 表在型︵詳しくは﹁大腸ポリープ﹂参照︶ 病変の肉眼的形態が軽度な隆起や陥凹を示すに過ぎないもの。 1型 腫瘤型 明らかに隆起した形態を示し、周囲粘膜との境界が明瞭なもの。 2型 潰瘍限局型 潰瘍を形成し、潰瘍をとりまく胃壁が肥厚し周堤を形成し、周堤と周囲粘膜との境界が比較的明瞭なもの。 3型 腫瘍浸潤型 潰瘍を形成し、腫瘍をとりまく胃壁が肥厚し周堤を形成するが、周堤と周囲粘膜との境界が不明瞭なもの。 4型 びまん浸潤型 著明な潰瘍形成も周堤もなく、胃壁の肥厚・硬化を特徴とし、病巣と周囲粘膜との境界が不明瞭なもの。 5型 分類不能 上記分類に当てはまらないもの。 という分類がある。これは胃癌の分類と全く同じである。大腸癌取り扱い規約によると壁深達度︵いわゆるT︶がTNM分類よりはるかに細かくなる。
その他の有名な分類[編集]
上記以外の有名な分類をあげる。どの分類を用いるか悩むときはなぜ分類するのかを考える。結局、治療の選択をしたいことが多いので自分がベストと思う治療法を選択する根拠となる分類を用いればよい。なお腸壁とは固有筋層までのことである。 Dukes分類 A:癌腫が腸壁内に限局するもの。 B:癌腫が腸壁を貫いて浸潤するがリンパ節転移がないもの。 C:リンパ節転移のあるもの。 Astler&Coller分類 A:癌腫が粘膜にとどまるもの。 B1:癌腫が固有筋層に及ぶがリンパ節転移のないもの。 B2:癌腫が固有筋層を穿通するが、リンパ節転移のないもの。 C1:癌腫が腸壁内に限局し、リンパ節転移のあるもの。 C2:癌腫が腸壁を穿通して外部に達し、リンパ節転移のあるもの。治療[編集]
他の癌の治療と同様に、治療方針は癌の病期によって変わってくる。主に以下に挙げられる治療を集学的に行っていく。また、近年では臨床診断が進み、大腸ポリープ・大腸癌を含めて﹁大腸腫瘍﹂として一括に取り扱うことで評価・治療を行っていく。本稿では大腸癌︵進行︶について主に記述。内視鏡治療[編集]
主に大腸ポリープ・早期大腸癌[注釈 2]に対し、内視鏡を用いてEMR・ESDによって病変切除による根治治療が施行される。内視鏡治療は原発巣の切除は可能であるが、リンパ節郭清は外科的手術でしか行えないため、リンパ節転移の無いと思われる病変に対し選択される。詳細は「大腸ポリープ」を参照
手術療法[編集]
旧来より、外科手術による癌病変切除・リンパ節郭清は根治術の根幹である。個々の術式に関しては﹁消化器外科学﹂参照。
他の悪性腫瘍と異なり、大腸や胃などの管腔臓器の癌は、癌による消化管閉塞︵イレウス︶・出血を生じることが多く、遠隔転移なども認める進行癌であっても、比較的全身状態良好なうちに食事摂取困難となる場合も多くあり、根治的ではなく対症療法的に原発巣切除・バイパス術施行などが行われることも多い。
詳細は「転移」を参照
化学療法[編集]
術後病期Stage Ⅲ以上の症例には再発予防のために6か月間の術後補助化学療法が実施される。フッ化ピリミジン系薬剤とオキサリプラチンの併用療法が推奨されているが、フッ化ピリミジン系薬剤単剤も選択肢となる。術後病期Stage IIの場合は、再発高リスク症例に対して同様の術後補助化学療法が検討される。
根治切除不能な進行再発大腸癌では、基本的に抗癌剤+分子標的治療薬という組み合わせの治療が適応とされている。大腸癌は「管腔臓器の腫瘍」であり、「出血」や「腸閉塞」と言った局所症状が強く出てくるため、原発巣切除治療が先行して行われる場合も多い。
- 抗癌剤
- 5-FU+フォリン酸(l-LV)
- イリノテカン(IRI)
- オキサリプラチン(OX)
- カペシタビン(Cape)
- S-1 (TS-1)
- UFT + フォリン酸
- S-1 + オキサリプラチン(SOX)
- カペシタビン + オキサリプラチン(CapeOX)
- S-1 + イリノテカン(IRIS)
- 5-FU + フォリン酸 + イリノテカン(FOLFIRI)
- 5-FU + フォリン酸 + オキサリプラチン(FOLFOX)
- 5-FU + フォリン酸 + オキサリプラチン + イリノテカン(FOLFOXIRI) - 「BRAF」遺伝子変異症例では化学療法不応の場合が多く「FOLFOXIRI + B-mab」が第一選択とされる。
- トリフルリジン(TAS-102):3次治療以降で単剤投与にて適応されている。
- 分子標的治療薬
血管新生阻害薬および抗EGFR抗体は上記の抗癌剤と併用して投与される。RASおよびBRAF変異の有無、一次治療か二次治療か、原発巣が左側か右側か、毒性プロファイルの違いなどからどちらの薬剤を併用するか検討される。併用薬剤としてベバシズマブとセツキシマブを比較した試験のサブグループ解析において、左側の場合はセツキシマブ、右側の場合はベバシズマブが優れた成績であった。
またBRAF変異陽性例の二次治療として、エンコラフェニブ(BRAF阻害薬)+MEK阻害薬(ビニメチニブ)+抗EGFR抗体(セツキシマブ)の併用療法の有効性が報告された。
- 血管新生阻害薬
- ベバシズマブ:(Bev:B-mab)血管内皮細胞増殖因子(VEGF)に対する抗体
- ラムシルマブ:(Ram)血管内皮細胞増殖因子受容体(VEGFR-2)に対する抗体 - 2次治療以降で「FOLFIRI]との併用でのみ適応
- アフリベルセプト:(Afl)血管内皮細胞増殖因子受容体(VEGFR-1.2.)に対する抗体 - 2次治療以降で「FOLFIRI]との併用でのみ適応
- 抗EGFR抗体
- マルチキナーゼ阻害薬
- BRAF阻害薬
- MEK阻害薬
免疫療法
大腸がんにはマイクロサテライト不安定性陽性症例(MSI-H)がおり、そのような症例には免疫療法が二次治療以降で行われる。
- 抗PD-1抗体
- ペムブロリズマブ
- ニボルマブ
- 抗CTLA-4抗体
- イピリムマブ
放射線療法[編集]
詳細は「放射線療法」を参照
特に直腸癌においては、原発腫瘍巣の縮小効果が大きく、手術での肛門機能温存も期待出来るため、第一選択として術前照射が広く行われている。
大腸癌にかかった人物[編集]
(アイウエオ順。生還者と亡くなった人物の双方を含む)
「Category:大腸癌で亡くなった人物」も参照
脚注[編集]
注釈[編集]
出典[編集]
(一)^ ab“Colon Cancer Treatment (PDQ®)”. NCI (2014年5月12日). 2014年7月5日時点のオリジナルよりアーカイブ。2014年6月29日閲覧。
(二)^ ab“General Information About Colon Cancer”. NCI (2014年5月12日). 2014年7月4日時点のオリジナルよりアーカイブ。2014年6月29日閲覧。
(三)^ “病気の起こり方も薬の副作用も男女で違う 見逃されてきた性差医療”. NHK (2023年4月28日). 2024年5月11日閲覧。
(四)^ abcdefghBosman, Frank T. (2014). “Chapter Chapter 5.5: Colorectal Cancer”. In Stewart, Bernard W.; Wild, Christopher P. World Cancer Report. the International Agency for Research on Cancer, World Health Organization. pp. 392-402. ISBN 978-92-832-0443-5  (五)^ ab“Colorectal Cancer Prevention (PDQ®)”. National Cancer Institute (2014年2月27日). 2014年7月5日時点のオリジナルよりアーカイブ。2014年6月29日閲覧。
(六)^ “阪神・原口選手が大腸がん20代の罹患は珍しいが怖がらず内視鏡検査を”. デイリースポーツ (2019年1月28日). 2021年10月3日閲覧。
(七)^ 大西淳子︵医学ジャーナリスト︶. “加糖飲料をよく飲む人は、大腸がんや腎臓がんの死亡リスクが上昇、”. 日経ビジネス電子版. 2023年2月13日閲覧。 “McCullough ML, et al. Cancer Epidemiol Biomarkers Prev. 2022 Oct 4;31(10):1907-1918.”
(八)^ Theodoratou E, Timofeeva M, Li X, Meng X, Ioannidis JP (August 2017). “Nature, Nurture, and Cancer Risks: Genetic and Nutritional Contributions to Cancer”. Annual Review of Nutrition 37: 293-320. doi:10.1146/annurev-nutr-071715-051004. PMC 6143166. PMID 28826375.
(九)^ abBibbins-Domingo K, Grossman DC, Curry SJ, Davidson KW, Epling JW, García FA, Gillman MW, Harper DM, Kemper AR, Krist AH, Kurth AE, Landefeld CS, Mangione CM, Owens DK, Phillips WR, Phipps MG, Pignone MP, Siu AL (June 2016). “Screening for Colorectal Cancer: US Preventive Services Task Force Recommendation Statement”. JAMA 315 (23): 2564-2575. doi:10.1001/jama.2016.5989. PMID 27304597.
(十)^ abForman, David; Ferlay, Jacques (2014). “Chapter Chapter 1.1: The global and regional burden of cancer”. In Stewart, Bernard W.; Wild, Christopher P. World Cancer Report. the International Agency for Research on Cancer, World Health Organization. pp. 16-53. ISBN 978-92-832-0443-5
(五)^ ab“Colorectal Cancer Prevention (PDQ®)”. National Cancer Institute (2014年2月27日). 2014年7月5日時点のオリジナルよりアーカイブ。2014年6月29日閲覧。
(六)^ “阪神・原口選手が大腸がん20代の罹患は珍しいが怖がらず内視鏡検査を”. デイリースポーツ (2019年1月28日). 2021年10月3日閲覧。
(七)^ 大西淳子︵医学ジャーナリスト︶. “加糖飲料をよく飲む人は、大腸がんや腎臓がんの死亡リスクが上昇、”. 日経ビジネス電子版. 2023年2月13日閲覧。 “McCullough ML, et al. Cancer Epidemiol Biomarkers Prev. 2022 Oct 4;31(10):1907-1918.”
(八)^ Theodoratou E, Timofeeva M, Li X, Meng X, Ioannidis JP (August 2017). “Nature, Nurture, and Cancer Risks: Genetic and Nutritional Contributions to Cancer”. Annual Review of Nutrition 37: 293-320. doi:10.1146/annurev-nutr-071715-051004. PMC 6143166. PMID 28826375.
(九)^ abBibbins-Domingo K, Grossman DC, Curry SJ, Davidson KW, Epling JW, García FA, Gillman MW, Harper DM, Kemper AR, Krist AH, Kurth AE, Landefeld CS, Mangione CM, Owens DK, Phillips WR, Phipps MG, Pignone MP, Siu AL (June 2016). “Screening for Colorectal Cancer: US Preventive Services Task Force Recommendation Statement”. JAMA 315 (23): 2564-2575. doi:10.1001/jama.2016.5989. PMID 27304597.
(十)^ abForman, David; Ferlay, Jacques (2014). “Chapter Chapter 1.1: The global and regional burden of cancer”. In Stewart, Bernard W.; Wild, Christopher P. World Cancer Report. the International Agency for Research on Cancer, World Health Organization. pp. 16-53. ISBN 978-92-832-0443-5  (11)^ “WHO Disease and injury country estimates”. World Health Organization (2009年). 2009年11月11日閲覧。
(12)^ Cunningham D, Atkin W, Lenz HJ, Lynch HT, Minsky B, Nordlinger B, Starling N (March 2010). “Colorectal cancer”. Lancet 375 (9719): 1030-1047. doi:10.1016/S0140-6736(10)60353-4. PMID 20304247.
(13)^ Lozano R, Naghavi M, Foreman K (December 2012). “Global and regional mortality from 235 causes of death for 20 age groups in 1990 and 2010: a systematic analysis for the Global Burden of Disease Study 2010”. Lancet 380 (9859): 2095-2128. doi:10.1016/S0140-6736(12)61728-0. PMID 23245604.
(14)^ がん統計白書2004
(15)^ 2015年のがん統計予測 (PDF)
(16)^ がん情報サービス﹁がん登録・統計﹂ (Report). 国立がん研究センター.
(17)^ 太田 昌幸︵千葉大学大学院医学研究院 診断病理学︶ (2020年). “癌取扱い規約の最近の変更点”. 癌取扱い規約の最近の変更点︵千葉県臨床検査技師会︶資料: 10︵検体の取扱い︶.
(18)^ 大腸がん検診について 日本対がん協会
(19)^ ﹁日本抗生物質学術協議会・ファイザー感染症研究助成海外留学報告会講演記録﹂﹃The Japanese Journal of Antibiotics.﹄Vol.58 (2005) No.2 p.179-199, doi:10.11553/antibiotics1968b.58.179, 日本感染症医薬品協会 より、大毛宏喜、竹末芳生、末田泰二郎﹃日本抗生物質学術協議会・ファイザー感染症研究助成海外留学報告会講演記録 -腸内硫化水素ガスー病因?ただの悪臭?-﹄2004年11月22日,学士会館203号
(20)^ ﹁硫化水素の細胞毒性の機構の解明﹂2009年度〜2011年度︵科学研究費助成事業データベース︶
(21)^ Ge Li, Dong-Heek Kim, Tae-Dong Kim, Byoung-Jeon Park,et al. (2004). “Protein-bound polysaccharide from Phellinus linteus induces G2/M phase arrest and apoptosis in SW480 human colon cancer cells”. Cancer Letters. 216: 175-181.
(22)^ 肥満指数・身長と大腸がんの関係について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(23)^ 赤肉・加工肉摂取量と大腸がん罹患リスクについて JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(24)^ World Cancer Research Fund and American Institute for Cancer Research (2007). Food, Nutrition, Physical Activity, and the Prevention of Cancer: A Global Perspective. Amer. Inst. for Cancer Research. ISBN 978-0972252225 日本語要旨‥食べもの、栄養、運動とがん予防 (PDF) 、世界がん研究基金と米国がん研究機構
(25)^ abお酒・たばこと大腸がんの関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(26)^ ビールロング缶1日1本で大腸がんの危険、女性は男性より少量・短期間でアルコール性肝硬変も(読売新聞2024年2月21日)
(27)^ 野菜・果物をよく食べると答えた人の大腸がん発症リスク
(28)^ 肉を良く食べると答えた人の、大腸がん発症リスク
(29)^ 食物繊維摂取と大腸がん罹患との関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(30)^ 米国国立がん研究所 (2006年9月1日). “Understanding Cancer Series: Cancer and the Environment”. 2009年12月1日閲覧。
(31)^ 食生活パターンと大腸がんとの関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(32)^ 篠原央、﹁[1]﹂﹃日本大腸肛門病学会雑誌﹄43巻1号 1990年 pp.33-43, doi:10.3862/jcoloproctology.43.33
(33)^ マグネシウム摂取と大腸がんとの関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(34)^ インスリン関連マーカーと大腸がん罹患との関係について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(35)^ 高感度CRP︵C反応性蛋白︶と大腸がん罹患との関係について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(36)^ 便潜血日本消化器病学会
(37)^ Timothy R. Church, Jack S. Mandel, Fred Ederer, Fecal Occult Blood Screening in the Minnesota Study: Sensitivity of the Screening Test, JNCI: Journal of the National Cancer Institute, Volume 89, Issue 19, 1 October 1997, Pages 1440–1448, doi:10.1093/jnci/89.19.1440.
(38)^ 高久 史磨﹃臨床検査データブック 2005~2006﹄医学書院 2005年
(39)^ 大腸癌スクリーニングにおける大腸内視鏡検査と免疫便潜血検査との比較
(40)^ 大腸がん検診受診と大腸がん死亡率との関係 JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(41)^ Winawer SJ, Zauber AG, Ho MN, et al. (December 1993). “Prevention of colorectal cancer by colonoscopic polypectomy. The National Polyp Study Workgroup”. N. Engl. J. Med. 329 (27): 1977-1981. doi:10.1056/NEJM199312303292701. PMID 8247072.
(42)^ Cummings, JH; Bingham SA (1998). “Diet and the prevention of cancer”. BMJ 317 (7173): 1636-1640. PMC 1114436. PMID 9848907.
(43)^ 身体活動量と大腸がん罹患との関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(44)^ 便通、便の状態と大腸がん罹患との関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(45)^ 野菜・果物摂取と大腸がんとの関係について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(46)^ Fuchs, C. S.; Giovannucci, EL; Colditz, GA; Hunter, DJ; Stampfer, MJ; Rosner, B; Speizer, FE; Willett, WC (1999). “Dietary Fiber and the Risk of Colorectal Cancer and Adenoma in Women”. New England Journal of Medicine 340 (340): 169-176. doi:10.1056/NEJM199901213400301. PMID 9895396.
(47)^ Baron, J. A.; Hunter, DJ; Spiegelman, D; Bergkvist, L; Berrino, F; Van Den Brandt, PA; Buring, JE; Colditz, GA et al. (2005). “Dietary Fiber and Colorectal Cancer: An Ongoing Saga”. Journal of the American Medical Association 294 (22): 2904-2906. doi:10.1001/jama.294.22.2904. PMID 16352792.
(48)^ “Health Effects of Eating Fiber”. 2008年8月21日時点のオリジナルよりアーカイブ。2010年6月8日閲覧。
(49)^ ab国立がんセンターがん対策情報センター (2009年2月25日). “日本人のためのがん予防法‥現状において推奨できる科学的根拠に基づくがん予防法”. 2009年12月1日閲覧。
(50)^ WHO technical report series 916. Diet, nutrition and the prevention of chronic diseases, 2003 & IARC monograph on the Evaluation of Carcinogenic Risks to Humans, Volume83, Tobacco Smoke and Involuntary Smoking, 2004
(51)^ “Vitamin D and Cancer Prevention: Strengths and Limits of the Evidence”. National Cancer Institute Fact Sheets. (2009年9月23日) 2010年6月17日閲覧。
(52)^ ビタミンDと大腸がん罹患との関係について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(53)^ Baron JA, Beach M, Mandel JS (1999). “Calcium supplements for the prevention of colorectal adenomas. Calcium Polyp Prevention Study Group”. N. Engl. J. Med. 340 (2): 101-107. doi:10.1056/NEJM199901143400204. PMID 9887161.
(54)^ Bonithon-Kopp C, Kronborg O, Giacosa A, Räth U, Faivre J (2000). “Calcium and fibre supplementation in prevention of colorectal adenoma recurrence: a randomised intervention trial. European Cancer Prevention Organisation Study Group”. Lancet 356 (9238): 1300-1306. doi:10.1016/S0140-6736(00)02813-0. PMID 11073017.
(55)^ Weingarten MA, Zalmanovici A, Yaphe J (2005). “Dietary calcium supplementation for preventing colorectal cancer, adenomatous polyps and calcium metabolisism disorder.”. Cochrane database of systematic reviews (Online) (3): CD003548. doi:10.1002/14651858.CD003548.pub3. PMID 16034903.
(56)^ カルシウム、ビタミンD摂取と大腸がん罹患との関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(57)^ Wactawski-Wende J, Kotchen JM, Anderson GL (2006). “Calcium plus vitamin D supplementation and the risk of colorectal cancer”. N. Engl. J. Med. 354 (7): 684-696. doi:10.1056/NEJMoa055222. PMID 16481636.
(58)^ n-3およびn-6不飽和脂肪酸摂取と大腸がんとの関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(59)^ 魚・n-3脂肪酸摂取と大腸がん罹患 JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(60)^ 葉酸、ビタミンB6、ビタミンB12、メチオニン摂取と大腸がん罹患との関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(61)^ コーヒー摂取と大腸がんとの関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(62)^ Seki, H.; Shiohara, M.; Matsumura, T.; Miyagawa, N.; Tanaka, M.; Komiyama, A.; Kurata, S. (February 2003). “Prevention of antibiotic-associated diarrhea in children by Clostridium butyricum MIYAIRI”. Pediatrics International 45 (1): 86-90. doi:10.1046/j.1442-200x.2003.01671.x. PMID 12654076.
(63)^ 黒岩豊秋, 小張一峰, 岩永正明﹁酪酸菌 (Clostridium butyricum MIYAIRI 588株) による腸管病原菌抑制作用﹂﹃感染症学雑誌﹄第64巻第3号、日本感染症学会、1990年、257-263頁、doi:10.11150/kansenshogakuzasshi1970.64.257。
(64)^ 伊藤寛﹁味噌のふくれと酪酸菌:クロストリジウム﹂﹃日本釀造協會雜誌﹄第63巻第4号、日本醸造協会、1968年、405-409頁、doi:10.6013/jbrewsocjapan1915.63.405、ISSN 0369-416X、NAID 130004110135。
(65)^ 佐々木雅也, 荒木克夫, 辻川知之, 安藤朗, 藤山佳秀﹁腸管細胞増殖と腸管フローラ﹂﹃腸内細菌学雑誌﹄第19巻第1号、日本ビフィズス菌センター、2005年1月、1-8頁、doi:10.11209/jim.19.1、ISSN 13430882、NAID 10019042772。
(66)^ 生田哲 ﹃バクテリアのはなし﹄︵日本実業出版 1999年2月25日︶p.188 ISBN 4-534-02902-0
(67)^ S.Y. Archer, et al., "P21 is required for butyrate-mediated growth inhibition of human colon cancer cells" Proc.Natl.Acad. Sci. USA vol.95 6791-6796 (1998), doi:10.1073/pnas.95.12.6791.
(68)^ 大河原壮, 古谷英樹, 長島康祐, 浅沼成人, 日野常男﹁酪酸生成菌 Butyrivibrio fibrisolvens の経口投与による実験的大腸癌形成の抑制﹂﹃ペット栄養学会誌﹄第8巻Supplement、日本ペット栄養学会、2005年、25-26頁、doi:10.11266/jpan1998.8.Supplement_25、ISSN 1344-3763、NAID 130004991169。
(69)^ 岩垣博巳, 日伝晶夫, 淵本定儀, 折田薫三, 米山勝, 堺修造﹁大腸癌患者と腸内細菌叢﹂﹃日本臨床外科医学会雑誌﹄第53巻第10号、日本臨床外科学会、1992年、2343-2346頁、doi:10.3919/ringe1963.53.2343、ISSN 0386-9776、NAID 130003597943。
(70)^ Katsoula A, et al., "Diagnostic Accuracy of Fecal Immunochemical Test in Patients at Increased Risk for Colorectal CancerA Meta-analysis" JAMA Intern Med. 2017 Aug 1;177(8):1110-1118, {{doi:10.1001/jamainternmed.2017.2309}}.
(71)^ Daniele Regge, Cristiana Laudi, Giovanni Galatola etal. Diagnostic Accuracy of Computed Tomographic Colonography for the Detection of Advanced Neoplasia in Individuals at Increased Risk of Colorectal Cancer. JAMA. 2009;301(23):2453-2461.
(72)^ ﹃INNERVISION︵インナービジョン︶﹄2001年10月号 / II CTコロノグラフィの技術動向/大腸仮想内視鏡‥大腸の新たな検査法 Virtual Colonoscopy‥An Alternative Approach to Examination of the Entire Colon Liang, J.Z.
(73)^ 唾液中のがんマーカーをわずか1分で測定する技術を開発-唾液検査で大腸がん患者を高精度かつ大規模に診断することが可能に-慶應義塾大学先端生命科学研究所プレスリリース︵2021年7月5日︶2021年8月21日閲覧
(74)^ abcdef大腸がん︵結腸がん・直腸がん︶ 国立がん研究センター がん情報サービス 更新・確認日‥2018年06月12日
(75)^ abc大腸がんの進行度分類︵ステージ︶と5年生存率 株式会社GCリンフォテック
(11)^ “WHO Disease and injury country estimates”. World Health Organization (2009年). 2009年11月11日閲覧。
(12)^ Cunningham D, Atkin W, Lenz HJ, Lynch HT, Minsky B, Nordlinger B, Starling N (March 2010). “Colorectal cancer”. Lancet 375 (9719): 1030-1047. doi:10.1016/S0140-6736(10)60353-4. PMID 20304247.
(13)^ Lozano R, Naghavi M, Foreman K (December 2012). “Global and regional mortality from 235 causes of death for 20 age groups in 1990 and 2010: a systematic analysis for the Global Burden of Disease Study 2010”. Lancet 380 (9859): 2095-2128. doi:10.1016/S0140-6736(12)61728-0. PMID 23245604.
(14)^ がん統計白書2004
(15)^ 2015年のがん統計予測 (PDF)
(16)^ がん情報サービス﹁がん登録・統計﹂ (Report). 国立がん研究センター.
(17)^ 太田 昌幸︵千葉大学大学院医学研究院 診断病理学︶ (2020年). “癌取扱い規約の最近の変更点”. 癌取扱い規約の最近の変更点︵千葉県臨床検査技師会︶資料: 10︵検体の取扱い︶.
(18)^ 大腸がん検診について 日本対がん協会
(19)^ ﹁日本抗生物質学術協議会・ファイザー感染症研究助成海外留学報告会講演記録﹂﹃The Japanese Journal of Antibiotics.﹄Vol.58 (2005) No.2 p.179-199, doi:10.11553/antibiotics1968b.58.179, 日本感染症医薬品協会 より、大毛宏喜、竹末芳生、末田泰二郎﹃日本抗生物質学術協議会・ファイザー感染症研究助成海外留学報告会講演記録 -腸内硫化水素ガスー病因?ただの悪臭?-﹄2004年11月22日,学士会館203号
(20)^ ﹁硫化水素の細胞毒性の機構の解明﹂2009年度〜2011年度︵科学研究費助成事業データベース︶
(21)^ Ge Li, Dong-Heek Kim, Tae-Dong Kim, Byoung-Jeon Park,et al. (2004). “Protein-bound polysaccharide from Phellinus linteus induces G2/M phase arrest and apoptosis in SW480 human colon cancer cells”. Cancer Letters. 216: 175-181.
(22)^ 肥満指数・身長と大腸がんの関係について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(23)^ 赤肉・加工肉摂取量と大腸がん罹患リスクについて JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(24)^ World Cancer Research Fund and American Institute for Cancer Research (2007). Food, Nutrition, Physical Activity, and the Prevention of Cancer: A Global Perspective. Amer. Inst. for Cancer Research. ISBN 978-0972252225 日本語要旨‥食べもの、栄養、運動とがん予防 (PDF) 、世界がん研究基金と米国がん研究機構
(25)^ abお酒・たばこと大腸がんの関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(26)^ ビールロング缶1日1本で大腸がんの危険、女性は男性より少量・短期間でアルコール性肝硬変も(読売新聞2024年2月21日)
(27)^ 野菜・果物をよく食べると答えた人の大腸がん発症リスク
(28)^ 肉を良く食べると答えた人の、大腸がん発症リスク
(29)^ 食物繊維摂取と大腸がん罹患との関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(30)^ 米国国立がん研究所 (2006年9月1日). “Understanding Cancer Series: Cancer and the Environment”. 2009年12月1日閲覧。
(31)^ 食生活パターンと大腸がんとの関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(32)^ 篠原央、﹁[1]﹂﹃日本大腸肛門病学会雑誌﹄43巻1号 1990年 pp.33-43, doi:10.3862/jcoloproctology.43.33
(33)^ マグネシウム摂取と大腸がんとの関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(34)^ インスリン関連マーカーと大腸がん罹患との関係について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(35)^ 高感度CRP︵C反応性蛋白︶と大腸がん罹患との関係について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(36)^ 便潜血日本消化器病学会
(37)^ Timothy R. Church, Jack S. Mandel, Fred Ederer, Fecal Occult Blood Screening in the Minnesota Study: Sensitivity of the Screening Test, JNCI: Journal of the National Cancer Institute, Volume 89, Issue 19, 1 October 1997, Pages 1440–1448, doi:10.1093/jnci/89.19.1440.
(38)^ 高久 史磨﹃臨床検査データブック 2005~2006﹄医学書院 2005年
(39)^ 大腸癌スクリーニングにおける大腸内視鏡検査と免疫便潜血検査との比較
(40)^ 大腸がん検診受診と大腸がん死亡率との関係 JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(41)^ Winawer SJ, Zauber AG, Ho MN, et al. (December 1993). “Prevention of colorectal cancer by colonoscopic polypectomy. The National Polyp Study Workgroup”. N. Engl. J. Med. 329 (27): 1977-1981. doi:10.1056/NEJM199312303292701. PMID 8247072.
(42)^ Cummings, JH; Bingham SA (1998). “Diet and the prevention of cancer”. BMJ 317 (7173): 1636-1640. PMC 1114436. PMID 9848907.
(43)^ 身体活動量と大腸がん罹患との関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(44)^ 便通、便の状態と大腸がん罹患との関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(45)^ 野菜・果物摂取と大腸がんとの関係について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(46)^ Fuchs, C. S.; Giovannucci, EL; Colditz, GA; Hunter, DJ; Stampfer, MJ; Rosner, B; Speizer, FE; Willett, WC (1999). “Dietary Fiber and the Risk of Colorectal Cancer and Adenoma in Women”. New England Journal of Medicine 340 (340): 169-176. doi:10.1056/NEJM199901213400301. PMID 9895396.
(47)^ Baron, J. A.; Hunter, DJ; Spiegelman, D; Bergkvist, L; Berrino, F; Van Den Brandt, PA; Buring, JE; Colditz, GA et al. (2005). “Dietary Fiber and Colorectal Cancer: An Ongoing Saga”. Journal of the American Medical Association 294 (22): 2904-2906. doi:10.1001/jama.294.22.2904. PMID 16352792.
(48)^ “Health Effects of Eating Fiber”. 2008年8月21日時点のオリジナルよりアーカイブ。2010年6月8日閲覧。
(49)^ ab国立がんセンターがん対策情報センター (2009年2月25日). “日本人のためのがん予防法‥現状において推奨できる科学的根拠に基づくがん予防法”. 2009年12月1日閲覧。
(50)^ WHO technical report series 916. Diet, nutrition and the prevention of chronic diseases, 2003 & IARC monograph on the Evaluation of Carcinogenic Risks to Humans, Volume83, Tobacco Smoke and Involuntary Smoking, 2004
(51)^ “Vitamin D and Cancer Prevention: Strengths and Limits of the Evidence”. National Cancer Institute Fact Sheets. (2009年9月23日) 2010年6月17日閲覧。
(52)^ ビタミンDと大腸がん罹患との関係について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(53)^ Baron JA, Beach M, Mandel JS (1999). “Calcium supplements for the prevention of colorectal adenomas. Calcium Polyp Prevention Study Group”. N. Engl. J. Med. 340 (2): 101-107. doi:10.1056/NEJM199901143400204. PMID 9887161.
(54)^ Bonithon-Kopp C, Kronborg O, Giacosa A, Räth U, Faivre J (2000). “Calcium and fibre supplementation in prevention of colorectal adenoma recurrence: a randomised intervention trial. European Cancer Prevention Organisation Study Group”. Lancet 356 (9238): 1300-1306. doi:10.1016/S0140-6736(00)02813-0. PMID 11073017.
(55)^ Weingarten MA, Zalmanovici A, Yaphe J (2005). “Dietary calcium supplementation for preventing colorectal cancer, adenomatous polyps and calcium metabolisism disorder.”. Cochrane database of systematic reviews (Online) (3): CD003548. doi:10.1002/14651858.CD003548.pub3. PMID 16034903.
(56)^ カルシウム、ビタミンD摂取と大腸がん罹患との関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(57)^ Wactawski-Wende J, Kotchen JM, Anderson GL (2006). “Calcium plus vitamin D supplementation and the risk of colorectal cancer”. N. Engl. J. Med. 354 (7): 684-696. doi:10.1056/NEJMoa055222. PMID 16481636.
(58)^ n-3およびn-6不飽和脂肪酸摂取と大腸がんとの関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(59)^ 魚・n-3脂肪酸摂取と大腸がん罹患 JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(60)^ 葉酸、ビタミンB6、ビタミンB12、メチオニン摂取と大腸がん罹患との関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(61)^ コーヒー摂取と大腸がんとの関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(62)^ Seki, H.; Shiohara, M.; Matsumura, T.; Miyagawa, N.; Tanaka, M.; Komiyama, A.; Kurata, S. (February 2003). “Prevention of antibiotic-associated diarrhea in children by Clostridium butyricum MIYAIRI”. Pediatrics International 45 (1): 86-90. doi:10.1046/j.1442-200x.2003.01671.x. PMID 12654076.
(63)^ 黒岩豊秋, 小張一峰, 岩永正明﹁酪酸菌 (Clostridium butyricum MIYAIRI 588株) による腸管病原菌抑制作用﹂﹃感染症学雑誌﹄第64巻第3号、日本感染症学会、1990年、257-263頁、doi:10.11150/kansenshogakuzasshi1970.64.257。
(64)^ 伊藤寛﹁味噌のふくれと酪酸菌:クロストリジウム﹂﹃日本釀造協會雜誌﹄第63巻第4号、日本醸造協会、1968年、405-409頁、doi:10.6013/jbrewsocjapan1915.63.405、ISSN 0369-416X、NAID 130004110135。
(65)^ 佐々木雅也, 荒木克夫, 辻川知之, 安藤朗, 藤山佳秀﹁腸管細胞増殖と腸管フローラ﹂﹃腸内細菌学雑誌﹄第19巻第1号、日本ビフィズス菌センター、2005年1月、1-8頁、doi:10.11209/jim.19.1、ISSN 13430882、NAID 10019042772。
(66)^ 生田哲 ﹃バクテリアのはなし﹄︵日本実業出版 1999年2月25日︶p.188 ISBN 4-534-02902-0
(67)^ S.Y. Archer, et al., "P21 is required for butyrate-mediated growth inhibition of human colon cancer cells" Proc.Natl.Acad. Sci. USA vol.95 6791-6796 (1998), doi:10.1073/pnas.95.12.6791.
(68)^ 大河原壮, 古谷英樹, 長島康祐, 浅沼成人, 日野常男﹁酪酸生成菌 Butyrivibrio fibrisolvens の経口投与による実験的大腸癌形成の抑制﹂﹃ペット栄養学会誌﹄第8巻Supplement、日本ペット栄養学会、2005年、25-26頁、doi:10.11266/jpan1998.8.Supplement_25、ISSN 1344-3763、NAID 130004991169。
(69)^ 岩垣博巳, 日伝晶夫, 淵本定儀, 折田薫三, 米山勝, 堺修造﹁大腸癌患者と腸内細菌叢﹂﹃日本臨床外科医学会雑誌﹄第53巻第10号、日本臨床外科学会、1992年、2343-2346頁、doi:10.3919/ringe1963.53.2343、ISSN 0386-9776、NAID 130003597943。
(70)^ Katsoula A, et al., "Diagnostic Accuracy of Fecal Immunochemical Test in Patients at Increased Risk for Colorectal CancerA Meta-analysis" JAMA Intern Med. 2017 Aug 1;177(8):1110-1118, {{doi:10.1001/jamainternmed.2017.2309}}.
(71)^ Daniele Regge, Cristiana Laudi, Giovanni Galatola etal. Diagnostic Accuracy of Computed Tomographic Colonography for the Detection of Advanced Neoplasia in Individuals at Increased Risk of Colorectal Cancer. JAMA. 2009;301(23):2453-2461.
(72)^ ﹃INNERVISION︵インナービジョン︶﹄2001年10月号 / II CTコロノグラフィの技術動向/大腸仮想内視鏡‥大腸の新たな検査法 Virtual Colonoscopy‥An Alternative Approach to Examination of the Entire Colon Liang, J.Z.
(73)^ 唾液中のがんマーカーをわずか1分で測定する技術を開発-唾液検査で大腸がん患者を高精度かつ大規模に診断することが可能に-慶應義塾大学先端生命科学研究所プレスリリース︵2021年7月5日︶2021年8月21日閲覧
(74)^ abcdef大腸がん︵結腸がん・直腸がん︶ 国立がん研究センター がん情報サービス 更新・確認日‥2018年06月12日
(75)^ abc大腸がんの進行度分類︵ステージ︶と5年生存率 株式会社GCリンフォテック
 (五)^ ab“Colorectal Cancer Prevention (PDQ®)”. National Cancer Institute (2014年2月27日). 2014年7月5日時点のオリジナルよりアーカイブ。2014年6月29日閲覧。
(六)^ “阪神・原口選手が大腸がん20代の罹患は珍しいが怖がらず内視鏡検査を”. デイリースポーツ (2019年1月28日). 2021年10月3日閲覧。
(七)^ 大西淳子︵医学ジャーナリスト︶. “加糖飲料をよく飲む人は、大腸がんや腎臓がんの死亡リスクが上昇、”. 日経ビジネス電子版. 2023年2月13日閲覧。 “McCullough ML, et al. Cancer Epidemiol Biomarkers Prev. 2022 Oct 4;31(10):1907-1918.”
(八)^ Theodoratou E, Timofeeva M, Li X, Meng X, Ioannidis JP (August 2017). “Nature, Nurture, and Cancer Risks: Genetic and Nutritional Contributions to Cancer”. Annual Review of Nutrition 37: 293-320. doi:10.1146/annurev-nutr-071715-051004. PMC 6143166. PMID 28826375.
(九)^ abBibbins-Domingo K, Grossman DC, Curry SJ, Davidson KW, Epling JW, García FA, Gillman MW, Harper DM, Kemper AR, Krist AH, Kurth AE, Landefeld CS, Mangione CM, Owens DK, Phillips WR, Phipps MG, Pignone MP, Siu AL (June 2016). “Screening for Colorectal Cancer: US Preventive Services Task Force Recommendation Statement”. JAMA 315 (23): 2564-2575. doi:10.1001/jama.2016.5989. PMID 27304597.
(十)^ abForman, David; Ferlay, Jacques (2014). “Chapter Chapter 1.1: The global and regional burden of cancer”. In Stewart, Bernard W.; Wild, Christopher P. World Cancer Report. the International Agency for Research on Cancer, World Health Organization. pp. 16-53. ISBN 978-92-832-0443-5
(五)^ ab“Colorectal Cancer Prevention (PDQ®)”. National Cancer Institute (2014年2月27日). 2014年7月5日時点のオリジナルよりアーカイブ。2014年6月29日閲覧。
(六)^ “阪神・原口選手が大腸がん20代の罹患は珍しいが怖がらず内視鏡検査を”. デイリースポーツ (2019年1月28日). 2021年10月3日閲覧。
(七)^ 大西淳子︵医学ジャーナリスト︶. “加糖飲料をよく飲む人は、大腸がんや腎臓がんの死亡リスクが上昇、”. 日経ビジネス電子版. 2023年2月13日閲覧。 “McCullough ML, et al. Cancer Epidemiol Biomarkers Prev. 2022 Oct 4;31(10):1907-1918.”
(八)^ Theodoratou E, Timofeeva M, Li X, Meng X, Ioannidis JP (August 2017). “Nature, Nurture, and Cancer Risks: Genetic and Nutritional Contributions to Cancer”. Annual Review of Nutrition 37: 293-320. doi:10.1146/annurev-nutr-071715-051004. PMC 6143166. PMID 28826375.
(九)^ abBibbins-Domingo K, Grossman DC, Curry SJ, Davidson KW, Epling JW, García FA, Gillman MW, Harper DM, Kemper AR, Krist AH, Kurth AE, Landefeld CS, Mangione CM, Owens DK, Phillips WR, Phipps MG, Pignone MP, Siu AL (June 2016). “Screening for Colorectal Cancer: US Preventive Services Task Force Recommendation Statement”. JAMA 315 (23): 2564-2575. doi:10.1001/jama.2016.5989. PMID 27304597.
(十)^ abForman, David; Ferlay, Jacques (2014). “Chapter Chapter 1.1: The global and regional burden of cancer”. In Stewart, Bernard W.; Wild, Christopher P. World Cancer Report. the International Agency for Research on Cancer, World Health Organization. pp. 16-53. ISBN 978-92-832-0443-5  (11)^ “WHO Disease and injury country estimates”. World Health Organization (2009年). 2009年11月11日閲覧。
(12)^ Cunningham D, Atkin W, Lenz HJ, Lynch HT, Minsky B, Nordlinger B, Starling N (March 2010). “Colorectal cancer”. Lancet 375 (9719): 1030-1047. doi:10.1016/S0140-6736(10)60353-4. PMID 20304247.
(13)^ Lozano R, Naghavi M, Foreman K (December 2012). “Global and regional mortality from 235 causes of death for 20 age groups in 1990 and 2010: a systematic analysis for the Global Burden of Disease Study 2010”. Lancet 380 (9859): 2095-2128. doi:10.1016/S0140-6736(12)61728-0. PMID 23245604.
(14)^ がん統計白書2004
(15)^ 2015年のがん統計予測 (PDF)
(16)^ がん情報サービス﹁がん登録・統計﹂ (Report). 国立がん研究センター.
(17)^ 太田 昌幸︵千葉大学大学院医学研究院 診断病理学︶ (2020年). “癌取扱い規約の最近の変更点”. 癌取扱い規約の最近の変更点︵千葉県臨床検査技師会︶資料: 10︵検体の取扱い︶.
(18)^ 大腸がん検診について 日本対がん協会
(19)^ ﹁日本抗生物質学術協議会・ファイザー感染症研究助成海外留学報告会講演記録﹂﹃The Japanese Journal of Antibiotics.﹄Vol.58 (2005) No.2 p.179-199, doi:10.11553/antibiotics1968b.58.179, 日本感染症医薬品協会 より、大毛宏喜、竹末芳生、末田泰二郎﹃日本抗生物質学術協議会・ファイザー感染症研究助成海外留学報告会講演記録 -腸内硫化水素ガスー病因?ただの悪臭?-﹄2004年11月22日,学士会館203号
(20)^ ﹁硫化水素の細胞毒性の機構の解明﹂2009年度〜2011年度︵科学研究費助成事業データベース︶
(21)^ Ge Li, Dong-Heek Kim, Tae-Dong Kim, Byoung-Jeon Park,et al. (2004). “Protein-bound polysaccharide from Phellinus linteus induces G2/M phase arrest and apoptosis in SW480 human colon cancer cells”. Cancer Letters. 216: 175-181.
(22)^ 肥満指数・身長と大腸がんの関係について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(23)^ 赤肉・加工肉摂取量と大腸がん罹患リスクについて JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(24)^ World Cancer Research Fund and American Institute for Cancer Research (2007). Food, Nutrition, Physical Activity, and the Prevention of Cancer: A Global Perspective. Amer. Inst. for Cancer Research. ISBN 978-0972252225 日本語要旨‥食べもの、栄養、運動とがん予防 (PDF) 、世界がん研究基金と米国がん研究機構
(25)^ abお酒・たばこと大腸がんの関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(26)^ ビールロング缶1日1本で大腸がんの危険、女性は男性より少量・短期間でアルコール性肝硬変も(読売新聞2024年2月21日)
(27)^ 野菜・果物をよく食べると答えた人の大腸がん発症リスク
(28)^ 肉を良く食べると答えた人の、大腸がん発症リスク
(29)^ 食物繊維摂取と大腸がん罹患との関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(30)^ 米国国立がん研究所 (2006年9月1日). “Understanding Cancer Series: Cancer and the Environment”. 2009年12月1日閲覧。
(31)^ 食生活パターンと大腸がんとの関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(32)^ 篠原央、﹁[1]﹂﹃日本大腸肛門病学会雑誌﹄43巻1号 1990年 pp.33-43, doi:10.3862/jcoloproctology.43.33
(33)^ マグネシウム摂取と大腸がんとの関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(34)^ インスリン関連マーカーと大腸がん罹患との関係について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(35)^ 高感度CRP︵C反応性蛋白︶と大腸がん罹患との関係について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(36)^ 便潜血日本消化器病学会
(37)^ Timothy R. Church, Jack S. Mandel, Fred Ederer, Fecal Occult Blood Screening in the Minnesota Study: Sensitivity of the Screening Test, JNCI: Journal of the National Cancer Institute, Volume 89, Issue 19, 1 October 1997, Pages 1440–1448, doi:10.1093/jnci/89.19.1440.
(38)^ 高久 史磨﹃臨床検査データブック 2005~2006﹄医学書院 2005年
(39)^ 大腸癌スクリーニングにおける大腸内視鏡検査と免疫便潜血検査との比較
(40)^ 大腸がん検診受診と大腸がん死亡率との関係 JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(41)^ Winawer SJ, Zauber AG, Ho MN, et al. (December 1993). “Prevention of colorectal cancer by colonoscopic polypectomy. The National Polyp Study Workgroup”. N. Engl. J. Med. 329 (27): 1977-1981. doi:10.1056/NEJM199312303292701. PMID 8247072.
(42)^ Cummings, JH; Bingham SA (1998). “Diet and the prevention of cancer”. BMJ 317 (7173): 1636-1640. PMC 1114436. PMID 9848907.
(43)^ 身体活動量と大腸がん罹患との関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(44)^ 便通、便の状態と大腸がん罹患との関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(45)^ 野菜・果物摂取と大腸がんとの関係について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(46)^ Fuchs, C. S.; Giovannucci, EL; Colditz, GA; Hunter, DJ; Stampfer, MJ; Rosner, B; Speizer, FE; Willett, WC (1999). “Dietary Fiber and the Risk of Colorectal Cancer and Adenoma in Women”. New England Journal of Medicine 340 (340): 169-176. doi:10.1056/NEJM199901213400301. PMID 9895396.
(47)^ Baron, J. A.; Hunter, DJ; Spiegelman, D; Bergkvist, L; Berrino, F; Van Den Brandt, PA; Buring, JE; Colditz, GA et al. (2005). “Dietary Fiber and Colorectal Cancer: An Ongoing Saga”. Journal of the American Medical Association 294 (22): 2904-2906. doi:10.1001/jama.294.22.2904. PMID 16352792.
(48)^ “Health Effects of Eating Fiber”. 2008年8月21日時点のオリジナルよりアーカイブ。2010年6月8日閲覧。
(49)^ ab国立がんセンターがん対策情報センター (2009年2月25日). “日本人のためのがん予防法‥現状において推奨できる科学的根拠に基づくがん予防法”. 2009年12月1日閲覧。
(50)^ WHO technical report series 916. Diet, nutrition and the prevention of chronic diseases, 2003 & IARC monograph on the Evaluation of Carcinogenic Risks to Humans, Volume83, Tobacco Smoke and Involuntary Smoking, 2004
(51)^ “Vitamin D and Cancer Prevention: Strengths and Limits of the Evidence”. National Cancer Institute Fact Sheets. (2009年9月23日) 2010年6月17日閲覧。
(52)^ ビタミンDと大腸がん罹患との関係について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(53)^ Baron JA, Beach M, Mandel JS (1999). “Calcium supplements for the prevention of colorectal adenomas. Calcium Polyp Prevention Study Group”. N. Engl. J. Med. 340 (2): 101-107. doi:10.1056/NEJM199901143400204. PMID 9887161.
(54)^ Bonithon-Kopp C, Kronborg O, Giacosa A, Räth U, Faivre J (2000). “Calcium and fibre supplementation in prevention of colorectal adenoma recurrence: a randomised intervention trial. European Cancer Prevention Organisation Study Group”. Lancet 356 (9238): 1300-1306. doi:10.1016/S0140-6736(00)02813-0. PMID 11073017.
(55)^ Weingarten MA, Zalmanovici A, Yaphe J (2005). “Dietary calcium supplementation for preventing colorectal cancer, adenomatous polyps and calcium metabolisism disorder.”. Cochrane database of systematic reviews (Online) (3): CD003548. doi:10.1002/14651858.CD003548.pub3. PMID 16034903.
(56)^ カルシウム、ビタミンD摂取と大腸がん罹患との関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(57)^ Wactawski-Wende J, Kotchen JM, Anderson GL (2006). “Calcium plus vitamin D supplementation and the risk of colorectal cancer”. N. Engl. J. Med. 354 (7): 684-696. doi:10.1056/NEJMoa055222. PMID 16481636.
(58)^ n-3およびn-6不飽和脂肪酸摂取と大腸がんとの関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(59)^ 魚・n-3脂肪酸摂取と大腸がん罹患 JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(60)^ 葉酸、ビタミンB6、ビタミンB12、メチオニン摂取と大腸がん罹患との関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(61)^ コーヒー摂取と大腸がんとの関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(62)^ Seki, H.; Shiohara, M.; Matsumura, T.; Miyagawa, N.; Tanaka, M.; Komiyama, A.; Kurata, S. (February 2003). “Prevention of antibiotic-associated diarrhea in children by Clostridium butyricum MIYAIRI”. Pediatrics International 45 (1): 86-90. doi:10.1046/j.1442-200x.2003.01671.x. PMID 12654076.
(63)^ 黒岩豊秋, 小張一峰, 岩永正明﹁酪酸菌 (Clostridium butyricum MIYAIRI 588株) による腸管病原菌抑制作用﹂﹃感染症学雑誌﹄第64巻第3号、日本感染症学会、1990年、257-263頁、doi:10.11150/kansenshogakuzasshi1970.64.257。
(64)^ 伊藤寛﹁味噌のふくれと酪酸菌:クロストリジウム﹂﹃日本釀造協會雜誌﹄第63巻第4号、日本醸造協会、1968年、405-409頁、doi:10.6013/jbrewsocjapan1915.63.405、ISSN 0369-416X、NAID 130004110135。
(65)^ 佐々木雅也, 荒木克夫, 辻川知之, 安藤朗, 藤山佳秀﹁腸管細胞増殖と腸管フローラ﹂﹃腸内細菌学雑誌﹄第19巻第1号、日本ビフィズス菌センター、2005年1月、1-8頁、doi:10.11209/jim.19.1、ISSN 13430882、NAID 10019042772。
(66)^ 生田哲 ﹃バクテリアのはなし﹄︵日本実業出版 1999年2月25日︶p.188 ISBN 4-534-02902-0
(67)^ S.Y. Archer, et al., "P21 is required for butyrate-mediated growth inhibition of human colon cancer cells" Proc.Natl.Acad. Sci. USA vol.95 6791-6796 (1998), doi:10.1073/pnas.95.12.6791.
(68)^ 大河原壮, 古谷英樹, 長島康祐, 浅沼成人, 日野常男﹁酪酸生成菌 Butyrivibrio fibrisolvens の経口投与による実験的大腸癌形成の抑制﹂﹃ペット栄養学会誌﹄第8巻Supplement、日本ペット栄養学会、2005年、25-26頁、doi:10.11266/jpan1998.8.Supplement_25、ISSN 1344-3763、NAID 130004991169。
(69)^ 岩垣博巳, 日伝晶夫, 淵本定儀, 折田薫三, 米山勝, 堺修造﹁大腸癌患者と腸内細菌叢﹂﹃日本臨床外科医学会雑誌﹄第53巻第10号、日本臨床外科学会、1992年、2343-2346頁、doi:10.3919/ringe1963.53.2343、ISSN 0386-9776、NAID 130003597943。
(70)^ Katsoula A, et al., "Diagnostic Accuracy of Fecal Immunochemical Test in Patients at Increased Risk for Colorectal CancerA Meta-analysis" JAMA Intern Med. 2017 Aug 1;177(8):1110-1118, {{doi:10.1001/jamainternmed.2017.2309}}.
(71)^ Daniele Regge, Cristiana Laudi, Giovanni Galatola etal. Diagnostic Accuracy of Computed Tomographic Colonography for the Detection of Advanced Neoplasia in Individuals at Increased Risk of Colorectal Cancer. JAMA. 2009;301(23):2453-2461.
(72)^ ﹃INNERVISION︵インナービジョン︶﹄2001年10月号 / II CTコロノグラフィの技術動向/大腸仮想内視鏡‥大腸の新たな検査法 Virtual Colonoscopy‥An Alternative Approach to Examination of the Entire Colon Liang, J.Z.
(73)^ 唾液中のがんマーカーをわずか1分で測定する技術を開発-唾液検査で大腸がん患者を高精度かつ大規模に診断することが可能に-慶應義塾大学先端生命科学研究所プレスリリース︵2021年7月5日︶2021年8月21日閲覧
(74)^ abcdef大腸がん︵結腸がん・直腸がん︶ 国立がん研究センター がん情報サービス 更新・確認日‥2018年06月12日
(75)^ abc大腸がんの進行度分類︵ステージ︶と5年生存率 株式会社GCリンフォテック
(11)^ “WHO Disease and injury country estimates”. World Health Organization (2009年). 2009年11月11日閲覧。
(12)^ Cunningham D, Atkin W, Lenz HJ, Lynch HT, Minsky B, Nordlinger B, Starling N (March 2010). “Colorectal cancer”. Lancet 375 (9719): 1030-1047. doi:10.1016/S0140-6736(10)60353-4. PMID 20304247.
(13)^ Lozano R, Naghavi M, Foreman K (December 2012). “Global and regional mortality from 235 causes of death for 20 age groups in 1990 and 2010: a systematic analysis for the Global Burden of Disease Study 2010”. Lancet 380 (9859): 2095-2128. doi:10.1016/S0140-6736(12)61728-0. PMID 23245604.
(14)^ がん統計白書2004
(15)^ 2015年のがん統計予測 (PDF)
(16)^ がん情報サービス﹁がん登録・統計﹂ (Report). 国立がん研究センター.
(17)^ 太田 昌幸︵千葉大学大学院医学研究院 診断病理学︶ (2020年). “癌取扱い規約の最近の変更点”. 癌取扱い規約の最近の変更点︵千葉県臨床検査技師会︶資料: 10︵検体の取扱い︶.
(18)^ 大腸がん検診について 日本対がん協会
(19)^ ﹁日本抗生物質学術協議会・ファイザー感染症研究助成海外留学報告会講演記録﹂﹃The Japanese Journal of Antibiotics.﹄Vol.58 (2005) No.2 p.179-199, doi:10.11553/antibiotics1968b.58.179, 日本感染症医薬品協会 より、大毛宏喜、竹末芳生、末田泰二郎﹃日本抗生物質学術協議会・ファイザー感染症研究助成海外留学報告会講演記録 -腸内硫化水素ガスー病因?ただの悪臭?-﹄2004年11月22日,学士会館203号
(20)^ ﹁硫化水素の細胞毒性の機構の解明﹂2009年度〜2011年度︵科学研究費助成事業データベース︶
(21)^ Ge Li, Dong-Heek Kim, Tae-Dong Kim, Byoung-Jeon Park,et al. (2004). “Protein-bound polysaccharide from Phellinus linteus induces G2/M phase arrest and apoptosis in SW480 human colon cancer cells”. Cancer Letters. 216: 175-181.
(22)^ 肥満指数・身長と大腸がんの関係について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(23)^ 赤肉・加工肉摂取量と大腸がん罹患リスクについて JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(24)^ World Cancer Research Fund and American Institute for Cancer Research (2007). Food, Nutrition, Physical Activity, and the Prevention of Cancer: A Global Perspective. Amer. Inst. for Cancer Research. ISBN 978-0972252225 日本語要旨‥食べもの、栄養、運動とがん予防 (PDF) 、世界がん研究基金と米国がん研究機構
(25)^ abお酒・たばこと大腸がんの関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(26)^ ビールロング缶1日1本で大腸がんの危険、女性は男性より少量・短期間でアルコール性肝硬変も(読売新聞2024年2月21日)
(27)^ 野菜・果物をよく食べると答えた人の大腸がん発症リスク
(28)^ 肉を良く食べると答えた人の、大腸がん発症リスク
(29)^ 食物繊維摂取と大腸がん罹患との関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(30)^ 米国国立がん研究所 (2006年9月1日). “Understanding Cancer Series: Cancer and the Environment”. 2009年12月1日閲覧。
(31)^ 食生活パターンと大腸がんとの関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(32)^ 篠原央、﹁[1]﹂﹃日本大腸肛門病学会雑誌﹄43巻1号 1990年 pp.33-43, doi:10.3862/jcoloproctology.43.33
(33)^ マグネシウム摂取と大腸がんとの関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(34)^ インスリン関連マーカーと大腸がん罹患との関係について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(35)^ 高感度CRP︵C反応性蛋白︶と大腸がん罹患との関係について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(36)^ 便潜血日本消化器病学会
(37)^ Timothy R. Church, Jack S. Mandel, Fred Ederer, Fecal Occult Blood Screening in the Minnesota Study: Sensitivity of the Screening Test, JNCI: Journal of the National Cancer Institute, Volume 89, Issue 19, 1 October 1997, Pages 1440–1448, doi:10.1093/jnci/89.19.1440.
(38)^ 高久 史磨﹃臨床検査データブック 2005~2006﹄医学書院 2005年
(39)^ 大腸癌スクリーニングにおける大腸内視鏡検査と免疫便潜血検査との比較
(40)^ 大腸がん検診受診と大腸がん死亡率との関係 JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(41)^ Winawer SJ, Zauber AG, Ho MN, et al. (December 1993). “Prevention of colorectal cancer by colonoscopic polypectomy. The National Polyp Study Workgroup”. N. Engl. J. Med. 329 (27): 1977-1981. doi:10.1056/NEJM199312303292701. PMID 8247072.
(42)^ Cummings, JH; Bingham SA (1998). “Diet and the prevention of cancer”. BMJ 317 (7173): 1636-1640. PMC 1114436. PMID 9848907.
(43)^ 身体活動量と大腸がん罹患との関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(44)^ 便通、便の状態と大腸がん罹患との関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(45)^ 野菜・果物摂取と大腸がんとの関係について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(46)^ Fuchs, C. S.; Giovannucci, EL; Colditz, GA; Hunter, DJ; Stampfer, MJ; Rosner, B; Speizer, FE; Willett, WC (1999). “Dietary Fiber and the Risk of Colorectal Cancer and Adenoma in Women”. New England Journal of Medicine 340 (340): 169-176. doi:10.1056/NEJM199901213400301. PMID 9895396.
(47)^ Baron, J. A.; Hunter, DJ; Spiegelman, D; Bergkvist, L; Berrino, F; Van Den Brandt, PA; Buring, JE; Colditz, GA et al. (2005). “Dietary Fiber and Colorectal Cancer: An Ongoing Saga”. Journal of the American Medical Association 294 (22): 2904-2906. doi:10.1001/jama.294.22.2904. PMID 16352792.
(48)^ “Health Effects of Eating Fiber”. 2008年8月21日時点のオリジナルよりアーカイブ。2010年6月8日閲覧。
(49)^ ab国立がんセンターがん対策情報センター (2009年2月25日). “日本人のためのがん予防法‥現状において推奨できる科学的根拠に基づくがん予防法”. 2009年12月1日閲覧。
(50)^ WHO technical report series 916. Diet, nutrition and the prevention of chronic diseases, 2003 & IARC monograph on the Evaluation of Carcinogenic Risks to Humans, Volume83, Tobacco Smoke and Involuntary Smoking, 2004
(51)^ “Vitamin D and Cancer Prevention: Strengths and Limits of the Evidence”. National Cancer Institute Fact Sheets. (2009年9月23日) 2010年6月17日閲覧。
(52)^ ビタミンDと大腸がん罹患との関係について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(53)^ Baron JA, Beach M, Mandel JS (1999). “Calcium supplements for the prevention of colorectal adenomas. Calcium Polyp Prevention Study Group”. N. Engl. J. Med. 340 (2): 101-107. doi:10.1056/NEJM199901143400204. PMID 9887161.
(54)^ Bonithon-Kopp C, Kronborg O, Giacosa A, Räth U, Faivre J (2000). “Calcium and fibre supplementation in prevention of colorectal adenoma recurrence: a randomised intervention trial. European Cancer Prevention Organisation Study Group”. Lancet 356 (9238): 1300-1306. doi:10.1016/S0140-6736(00)02813-0. PMID 11073017.
(55)^ Weingarten MA, Zalmanovici A, Yaphe J (2005). “Dietary calcium supplementation for preventing colorectal cancer, adenomatous polyps and calcium metabolisism disorder.”. Cochrane database of systematic reviews (Online) (3): CD003548. doi:10.1002/14651858.CD003548.pub3. PMID 16034903.
(56)^ カルシウム、ビタミンD摂取と大腸がん罹患との関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(57)^ Wactawski-Wende J, Kotchen JM, Anderson GL (2006). “Calcium plus vitamin D supplementation and the risk of colorectal cancer”. N. Engl. J. Med. 354 (7): 684-696. doi:10.1056/NEJMoa055222. PMID 16481636.
(58)^ n-3およびn-6不飽和脂肪酸摂取と大腸がんとの関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(59)^ 魚・n-3脂肪酸摂取と大腸がん罹患 JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(60)^ 葉酸、ビタミンB6、ビタミンB12、メチオニン摂取と大腸がん罹患との関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(61)^ コーヒー摂取と大腸がんとの関連について JPHC Study 多目的コホート研究 独立行政法人国立がん研究センター
(62)^ Seki, H.; Shiohara, M.; Matsumura, T.; Miyagawa, N.; Tanaka, M.; Komiyama, A.; Kurata, S. (February 2003). “Prevention of antibiotic-associated diarrhea in children by Clostridium butyricum MIYAIRI”. Pediatrics International 45 (1): 86-90. doi:10.1046/j.1442-200x.2003.01671.x. PMID 12654076.
(63)^ 黒岩豊秋, 小張一峰, 岩永正明﹁酪酸菌 (Clostridium butyricum MIYAIRI 588株) による腸管病原菌抑制作用﹂﹃感染症学雑誌﹄第64巻第3号、日本感染症学会、1990年、257-263頁、doi:10.11150/kansenshogakuzasshi1970.64.257。
(64)^ 伊藤寛﹁味噌のふくれと酪酸菌:クロストリジウム﹂﹃日本釀造協會雜誌﹄第63巻第4号、日本醸造協会、1968年、405-409頁、doi:10.6013/jbrewsocjapan1915.63.405、ISSN 0369-416X、NAID 130004110135。
(65)^ 佐々木雅也, 荒木克夫, 辻川知之, 安藤朗, 藤山佳秀﹁腸管細胞増殖と腸管フローラ﹂﹃腸内細菌学雑誌﹄第19巻第1号、日本ビフィズス菌センター、2005年1月、1-8頁、doi:10.11209/jim.19.1、ISSN 13430882、NAID 10019042772。
(66)^ 生田哲 ﹃バクテリアのはなし﹄︵日本実業出版 1999年2月25日︶p.188 ISBN 4-534-02902-0
(67)^ S.Y. Archer, et al., "P21 is required for butyrate-mediated growth inhibition of human colon cancer cells" Proc.Natl.Acad. Sci. USA vol.95 6791-6796 (1998), doi:10.1073/pnas.95.12.6791.
(68)^ 大河原壮, 古谷英樹, 長島康祐, 浅沼成人, 日野常男﹁酪酸生成菌 Butyrivibrio fibrisolvens の経口投与による実験的大腸癌形成の抑制﹂﹃ペット栄養学会誌﹄第8巻Supplement、日本ペット栄養学会、2005年、25-26頁、doi:10.11266/jpan1998.8.Supplement_25、ISSN 1344-3763、NAID 130004991169。
(69)^ 岩垣博巳, 日伝晶夫, 淵本定儀, 折田薫三, 米山勝, 堺修造﹁大腸癌患者と腸内細菌叢﹂﹃日本臨床外科医学会雑誌﹄第53巻第10号、日本臨床外科学会、1992年、2343-2346頁、doi:10.3919/ringe1963.53.2343、ISSN 0386-9776、NAID 130003597943。
(70)^ Katsoula A, et al., "Diagnostic Accuracy of Fecal Immunochemical Test in Patients at Increased Risk for Colorectal CancerA Meta-analysis" JAMA Intern Med. 2017 Aug 1;177(8):1110-1118, {{doi:10.1001/jamainternmed.2017.2309}}.
(71)^ Daniele Regge, Cristiana Laudi, Giovanni Galatola etal. Diagnostic Accuracy of Computed Tomographic Colonography for the Detection of Advanced Neoplasia in Individuals at Increased Risk of Colorectal Cancer. JAMA. 2009;301(23):2453-2461.
(72)^ ﹃INNERVISION︵インナービジョン︶﹄2001年10月号 / II CTコロノグラフィの技術動向/大腸仮想内視鏡‥大腸の新たな検査法 Virtual Colonoscopy‥An Alternative Approach to Examination of the Entire Colon Liang, J.Z.
(73)^ 唾液中のがんマーカーをわずか1分で測定する技術を開発-唾液検査で大腸がん患者を高精度かつ大規模に診断することが可能に-慶應義塾大学先端生命科学研究所プレスリリース︵2021年7月5日︶2021年8月21日閲覧
(74)^ abcdef大腸がん︵結腸がん・直腸がん︶ 国立がん研究センター がん情報サービス 更新・確認日‥2018年06月12日
(75)^ abc大腸がんの進行度分類︵ステージ︶と5年生存率 株式会社GCリンフォテック
参考文献[編集]
- 『大腸癌治療ガイドライン2005年版』大腸癌研究会(Minds医療情報サービス)
- 『大腸癌治療ガイドライン医師用2010年版』大腸癌研究会(Minds医療情報サービス)
- 『有効性評価に基づく大腸がん検診ガイドライン2005年版』厚生労働省がん研究班編 (Minds医療情報サービス)
- 『大腸癌取扱い規約 2006年3月【第7版】』 大腸癌研究会 編、金原出版
- 『大腸がん標準化学療法の実際 改訂第2版』金原出版 (2009年1月) ISBN 978-4307101431
- 松野正紀監修『改訂版 消化器外科手術のため解剖学 小腸・大腸、肛門部疾患、肝臓・胆嚢・胆道系、膵臓・脾臓』メジカルビュー社 2007年 ISBN 978-4-7583-0323-1
関連項目[編集]
外部リンク[編集]
- がん検診ガイドライン 大腸がん - 国立がんセンター
- がん情報サイト Cancer Information Japan -(米国国立がん研究所によるPDQの日本語版)
- 大腸がん - 国立がん研究所がん情報サービス(一般の方向けサイト)2016年01月06日更新、2018年01月21日閲覧
- 「見つかりにくい」大腸がん特集…こんな症状には注意 (読売新聞2015年10月1日)
- 大腸がんの転移が進み、手術もできなかった友を救った薬とは (読売新聞2023年9月13日)
- 日本人に最も多い大腸がん、悪化させる体内物質を特定…京都大などの研究チーム (読売新聞2023年9月27日)
- 歯周病、大腸がんに関係か 国内外で相次ぐ研究報告 早期治療がメリット大 (47NEWS、共同通信、2024年04月30日)